Однією
з основних проблем фізики нашого і минулого століття вважається пояснення
макроскопічних властивостей твердих тіл на основі квантової теорії атомів, з
яких ці тіла складаються. Задачу можна буде вважати успішно розв’язаною, якщо
стане можливим, знаючи склад речовини, теоретично розрахувати її основні
характеристики і їх поведінку при зміні зовнішніх умов. В принципі точні
розрахунки можливі уже і в сучасний час, так як сили взаємодії між частинками
речовини відомі, а основні положення квантової механіки і квантової статистики
твердо встановлені. Але на практиці суворий підхід до проблеми призводить до
складних, математично нерозв’язних задач. Тому користуються спрощеними та
ідеалізованими моделями.
З квантової
механіки відомо, що для теоретичного дослідження будь-якої системи частинок,
знаходження можливих значень її енергії, потрібно розв’язати вихідне рівняння Шредінгера:
![]() . (1)
. (1)
Розв’язок цього
рівняння дав би можливість отримати всі необхідні відомості про систему:
дозволені значення енергії, конфігурацію ядер,
просторовий розподіл електронів і т. д. Проте це рівняння має стільки змінних,
скільки ступенів вільності має досліджувана система. Якщо такою системою є
тверде тіло, то слід брати до уваги всі атомні ядра та електрони. Енергії
названих частинок включає в себе Ĥ
- оператор Гамільтона:
а) кінетичну енергію електронів;
б) кінетичну енергію ядер;
в) потенціальну енергію попарної взаємодії
електронів між собою;
г) потенціальну енергію попарної взаємодії ядер між собою;
д) потенціальну енергію взаємодії електронів з
ядрами.
Відомо, що число одних тільки атомів у твердому
тілі становить ~1023 в 1см3. Отже, число ступенів
вільності, а з ним і число змінних у згаданому рівнянні буде також порядку 1023
– 1024. Прямий, безпосередній розв’язок рівняння із 1023
змінними нині неможливий. Проте, якби навіть і вдалось розв’язати це рівняння з
таким числом змінних, то був би отриманий такий об’єм інформації, фізична інтерпритація якої викликала б значні труднощі.
В зв’язку з цим
квантову теорію твердого тіла розглядають на основі деяких спрощень:
1. При вивченні руху
електронів атомні ядра внаслідок їх значної масивності, розглядаються як
нерухомі джерела поля, що діє на електрони. Тому кінетична енергія ядер при такому допущенні стає рівною нулеві. Це наближення
називається адіабатичним або наближенням Борна-Оппенгеймера
і дозволяє зменшити число змінних у рівнянні Шредінгера.
2. Розміщення ядер у просторі вважається строго періодичним: вони розміщуються
у вузлах ідеальної гратки цього кристалу. Це
зауваження обмежує клас розглядуваних систем: досліджуються саме кристалічні
тверді тіла, а не рідини, скло і т. п.
3. Взаємодія електронів
одного з одним замінюється деяким ефективним зовнішнім полем. Інакше кажучи,
система електронів, які взаємодіють з атомними ядрами і один з одним згідно
закону Кулона, замінюється системою незалежних електронів, що рухаються в
деякому заданому полі. Останнє складається із поля атомних ядер
і ефективного поля всіх електронів. Це поле не тільки впливає на рух такого
електрона, але і електрон впливає на все поле. Тому воно називається самоузгодженим, а такий метод
розв’язання багатоелектронної задачі – методом Хартрі-Фока.
Таким чином, третє допущення зводить багатоелектронну задачу до одноелектронної.
Замість одного рівняння Шредінгера для всієї системи
атомних ядер і електронів, ми отримуємо сукупність ідентичнних, не зв’язаних між собою рівнянь Шредінгера для кожного електрона окремо.
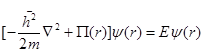 , (
, (![]() )
)
де ![]() - кінетична енергія
електрона і
- кінетична енергія
електрона і ![]() ;
;
![]() - потенціальна енергія
електрона в кристалі;
- потенціальна енергія
електрона в кристалі;
![]() - повна енергія
електрона;
- повна енергія
електрона;
![]() - хвильова функція елекрона.
- хвильова функція елекрона.
Розв’язки
таких спрощених рівнянь Шредінгера типу (1) дають
відомості про енергетичний спектр електронів, які рухаються в періодичному полі
кристалу. Цей спектр являє собою сукупність інтервалів енергій, які називаються
енергетичними законами. Тому розглянута нами якісно і спрощено теорія
називається зонною теорією. Її основи були закладені німецьким фізиком Блохом (1928 р.) та французьким фізиком Бриллюеном
(1930 р.).
Отже, в основу зонної теорії покладено зведення багатоелектронної задачі до задачі одноелектронної.
Зонна теорія – теорія одного електрона; це її перша риса. Другою характерною
рисою зонної теорії є певне допущення про характер силового поля, в якому
рухається кожний окремий електрон; це поле періодичне в просторі та його
періоди збігаються з періодами гратки. Періодичне
поле являє собою послідовне чергування однакових потенціальних бар’єрів і ям.
Як видно, тільки
суто теоретичний розгляд твердого тіла призводить до існування його
енергетичної зонної структури. Знання про електронний енергетичний спектр
твердих тіл дає можливість визначити, буде речовина металом, чи ізолятором,
якою енергією вона характеризується і т. д. Експерементальним
підтвердженням правильності розрахунків зонної структури матеріалів є досліди
по циклотронному резонансу, інфрачервоному поглинанню, гальваномагнітних
ефектах і т. д.
Електронні стани в
твердих тілах мають суттєву схожість зі станами електронів у вільних атомах,
оскільки взаємодії між електронами сусідніх атомів не можуть повністю
зруйнувати вихідну структуру електронних рівнів окремих атомів. Слід сказати,
що взаємодії між атомами в кристалі є досить- таки сильними і достатні для того, щоб серйозно вплинути на
енергетичні рівні окремих атомів.
Розглянемо спочатку електронний енергетичний
спектр окремого ізольованого атома.
В ізольованому атомі енергетичні рівні мають
дискретний набір енергій:
![]() , (2)
, (2)
де n=1,2,3,…. Наприклад атом водню має
енергетичну структуру, показану на рис. 1. Число n (номер енергетичного рівня)
називається головним квантовим числом. Від нього в основному залежить
енергія електрона (2) в атомі. Воно набуває тільки цілочислові значення від 1 до
∞. В теорії Бора це число визначає радіус орбіти електрона в атомі (точніше розміри великої півосі еліптичної орбіти електрона), тобто це є порядковий
номер дозволеної орбіти, або енергетичного рівня електрона. В теорії Бора
припускається, що електронні орбіти можуть бути лише коловими, проте при
дальшому розвитку ідей Бора Зоммерфельд дійшов
висновку, що можуть існувати не тільки колові, але й еліптичні орбіти.
Розрахунки Зоммерфельда показали, що в одному й тому
ж стані атома водню, який, як і в теорії Бора, визначається головним квантовим
числом n, можуть відповідати орбіти різної форми, кожна з яких зв’язана з
певним значенням орбітального моменту кількості руху.
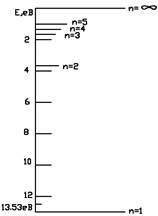
Рис.1. Енергетичний спектр вільного
атома водню
Звідси випливає, що для характеристики поведінки електрона в
атомі одного квантового числа n вже не досить. Його доцільно залишити для
характеристики енергії стаціонарного стану, а для характеристики орбітального
моменту кількості руху треба ввести додатково орбітальне квантове число ![]() .
.
Орбітальне (азимутальне або побічне)
квантове число ![]() визначає орбітальний момент кількості руху електрона
визначає орбітальний момент кількості руху електрона
![]() .
(3)
.
(3)
Воно може набувати тільки цілочислових значень
від 0 до n-1, де n-головне квантове число. За теорією Бора ![]() визначало
ексцентриситет еліптичної орбіти. Орбіта буде коло при
визначало
ексцентриситет еліптичної орбіти. Орбіта буде коло при ![]() = n-1, при всіх інших
значеннях
= n-1, при всіх інших
значеннях ![]() орбіти будуть
еліптичними. Еліптичність орбіти електрона в атомі водню не впливає на значення
енергії рівня, але в більш складних атомах при великому ексцентриситеті такий
вплив спостерігається. Отже, енергія рівня починає залежати і від значення
орбіти будуть
еліптичними. Еліптичність орбіти електрона в атомі водню не впливає на значення
енергії рівня, але в більш складних атомах при великому ексцентриситеті такий
вплив спостерігається. Отже, енергія рівня починає залежати і від значення ![]() . Енергетичний стан, що характирезуються
значенням
. Енергетичний стан, що характирезуються
значенням ![]() називається s-станом.
Відповідно для
називається s-станом.
Відповідно для ![]() =1-p-станом,
=1-p-станом, ![]() =2-d-станом,
=2-d-станом, ![]() =3 -f- станом,
=3 -f- станом, ![]() =4 -g- стани,
=4 -g- стани, ![]() =5 -h- стани і т.д.
=5 -h- стани і т.д.
Для пояснення змін у спектрах випромінювання
атомів різних хімічних елементів, які спричиняються дією електричних і
магнітних полів, вводять ще два квантові числа. Одне з них – магнітне квантове исло
![]() , що визначає величини проекцій орбітальних механічного і
магнітного моментів на заданий напрям, наприклад, напрям зовнішнього магнітного
поля
, що визначає величини проекцій орбітальних механічного і
магнітного моментів на заданий напрям, наприклад, напрям зовнішнього магнітного
поля ![]() (4). У теорії Бора
(4). У теорії Бора ![]() визначало орієнтування
електронної оболонки в просторі. Проекція вектора
моменту кількості руху (а отже, і вектора магнітного
моменту, створюваного рухом електрона по орбіті) на виділений напрям може мати
не будь-яке значення, а тільки деякі дискретні значення, що визначаються
магнітним квантовим числом. Магнітне квантове число
визначало орієнтування
електронної оболонки в просторі. Проекція вектора
моменту кількості руху (а отже, і вектора магнітного
моменту, створюваного рухом електрона по орбіті) на виділений напрям може мати
не будь-яке значення, а тільки деякі дискретні значення, що визначаються
магнітним квантовим числом. Магнітне квантове число ![]() може набувати всіх
цілих значень (включаючи нуль) від -l до +l, тобто 2
може набувати всіх
цілих значень (включаючи нуль) від -l до +l, тобто 2![]() +1 різних значень при цьому самому значенні орбітального
квантового числа l. Наприклад, при l =4, магнітне квантове число може
дорівнювати -4,-3,-2,-1,0,+1,+2,+3,+4. Отже, при даних n i l електрон в атомі,
що перебуває в магнітному полі, може рухатися по 2
+1 різних значень при цьому самому значенні орбітального
квантового числа l. Наприклад, при l =4, магнітне квантове число може
дорівнювати -4,-3,-2,-1,0,+1,+2,+3,+4. Отже, при даних n i l електрон в атомі,
що перебуває в магнітному полі, може рухатися по 2![]() +1 орбітах, які відрізняються своєю орієнтацією напрямку
магнітного поля. Ще одним квантовим числом, яке характеризує
виключно особливості самого електрона є спінове
квантове число
+1 орбітах, які відрізняються своєю орієнтацією напрямку
магнітного поля. Ще одним квантовим числом, яке характеризує
виключно особливості самого електрона є спінове
квантове число![]() . Електрон характеризується не лише зарядом і масою, а й певним власним моментом кількості руху,
який дістав назву "спіну", і зв'язаним з
ним власним магнітним моментом. Вектор цієї величини може мати один із двох
напрямів: або цей вектор паралельний вектору орбітального моменту кількості
руху, або ж антипаралельний йому. Отже, спінове квантове число
. Електрон характеризується не лише зарядом і масою, а й певним власним моментом кількості руху,
який дістав назву "спіну", і зв'язаним з
ним власним магнітним моментом. Вектор цієї величини може мати один із двох
напрямів: або цей вектор паралельний вектору орбітального моменту кількості
руху, або ж антипаралельний йому. Отже, спінове квантове число![]() може набувати двох
різних значень
може набувати двох
різних значень ![]() і
і ![]() для кожного значення магнітного квантового числа
для кожного значення магнітного квантового числа ![]() .
.
Просто кажучи, це спінове число визначає напрям обертання
електрона навколо власної осі.
Отже, стан кожного електрона в атомі характеризується чотирма
квантовими числами. Енергія стану електрона в атомі залежить в основному від
чисел![]() і
і![]() , хоча існує незначна залежність енергії й від числа
, хоча існує незначна залежність енергії й від числа ![]() . Енергія стану сильніше зростає із збільшенням n, ніж із
збільшенням числа
. Енергія стану сильніше зростає із збільшенням n, ніж із
збільшенням числа ![]() . Тому, як правило, стан із більшим n має, незалежно від
значення l, більшу енергію. Сукупність електронів з одним і тим самим значенням
головного квантового числа n утворює оболонку
(шар) атома. Для n =1 маємо К - оболонку, n =2 - L - оболонка, n =3 - M
- оболонка і т.д. Кожна оболонка характеризується
станами орбітального руху (s,p,d,...) електронів,
кожна оболонка складається із підоболонок, яким
відповідають свої значення орбітального квантового числа
. Тому, як правило, стан із більшим n має, незалежно від
значення l, більшу енергію. Сукупність електронів з одним і тим самим значенням
головного квантового числа n утворює оболонку
(шар) атома. Для n =1 маємо К - оболонку, n =2 - L - оболонка, n =3 - M
- оболонка і т.д. Кожна оболонка характеризується
станами орбітального руху (s,p,d,...) електронів,
кожна оболонка складається із підоболонок, яким
відповідають свої значення орбітального квантового числа ![]() . При даному
. При даному ![]() магнітне квантове
число має 2
магнітне квантове
число має 2![]() +1 значень, Отже, максимальне число електронів в даній під
оболонці рівне
+1 значень, Отже, максимальне число електронів в даній під
оболонці рівне ![]()
![]() . Усі ці електрони мають однакові значення n i
. Усі ці електрони мають однакові значення n i ![]() . Максимальне число електронів, які мають дане головне число
n, або максимальне число електронів у цій оболонці буде
. Максимальне число електронів, які мають дане головне число
n, або максимальне число електронів у цій оболонці буде
![]()
![]() . (5)
. (5)
Таким чином, в атомі не
може існувати більш як 2n2 електронів з однаковими квантовими
числами n. Наведені вище маркування можна узагальнити у вигляді таблиці
Таблиця 1
|
Оболонка |
n |
0 s |
1 p |
2 d |
3 f |
4 g |
Всього
електронів 2n2 |
|
K |
1 |
2 |
- |
- |
- |
- |
2 |
|
L |
2 |
2 |
6 |
- |
- |
- |
8 |
|
M |
3 |
2 |
6 |
10 |
- |
- |
18 |
|
N |
4 |
2 |
6 |
10 |
14 |
- |
32 |
|
O |
5 |
2 |
6 |
10 |
14 |
18 |
50 |
З таблиці 1 видно, що в К - оболонці може знаходитися максимум 2
електрони, в L - оболонці - 8, в М - 18 електронів і т.д.
Аналогічно, в s -підоболонці максимальне число електронів 2, в р. - 6, d -
Такий розподіл електронів по станах в атомі відповідає принципу
Паулі, згідно якого: в одному квантовому
стані, що характеризується чотирма квантовими числами, може знаходитися не
більше одного електрона. Відповідно у квантовому стані, що визначається
трьома квантовими числами ![]() може знаходитись не
більше двох електронів з антипаралельними спінами
може знаходитись не
більше двох електронів з антипаралельними спінами ![]() . Якби принцип Паулі не діяв, то всі електрони перейшли б у
стан 1s, оскільки всяка система намагається бути в стані з найменшою енергією.
. Якби принцип Паулі не діяв, то всі електрони перейшли б у
стан 1s, оскільки всяка система намагається бути в стані з найменшою енергією.
З попереднього видно,
що у кожному s - стані знаходиться не більше двох електронів із протилежно
направленими спінами. Усі s - рівні є, таким чином невиродженими, якщо не
враховувати виродження по спіну. Нагадаємо, що стан
буде невиродженим тоді, коли в ньому знаходиться два з протилежними спінами електрони. Відповідно, якщо в стані розміщено
більше двох електронів, то він стає виродженим.
Отже, p -, d -, f - і т. д. стани є виродженими. Кратність виродження
знаходиться з виразу ![]() , і тому р, - стани трикратно вироджені , d - стани - п'ятикратно вироджені і т. д. В загальному випадку рівень з
орбітальним квантовим числом
, і тому р, - стани трикратно вироджені , d - стани - п'ятикратно вироджені і т. д. В загальному випадку рівень з
орбітальним квантовим числом ![]() має
має ![]() - кратне виродження і на ньому може розміститись
- кратне виродження і на ньому може розміститись ![]() електронів. Так як енергія даного рівня визначається
квантовими числами n i
електронів. Так як енергія даного рівня визначається
квантовими числами n i ![]() , то це означає, що всі
, то це означає, що всі ![]() електронів мають одну
і ту ж енергію. При дії на вільний атом сильного зовнішнього поля виродження
його рівнів знімається: кожен із них розщеплюється на
електронів мають одну
і ту ж енергію. При дії на вільний атом сильного зовнішнього поля виродження
його рівнів знімається: кожен із них розщеплюється на![]() близько розміщених підрівнів, що показано в таблиці 2.
близько розміщених підрівнів, що показано в таблиці 2.
Таблиця 2
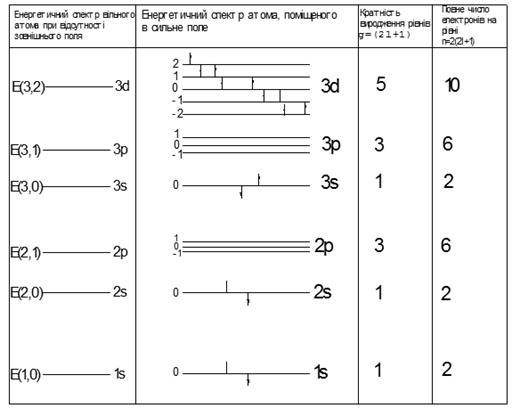
В таблиці на підрівнях 2р і 3р спіни електронів
не показані.
На різні рівні атома зовнішнє поле діє
неоднаково. Внутрішні електрони сильно зв’язані з ядром і тому майже не
відчувають впливу зовнішнього поля, внаслідок чого відповідні їм рівні
розщеплюються слабо. По мірі переходу до зовнішніх електронів їх, степінь
взаємодії з ядром зменшується через дві причини: вони стають більш віддаленими
від ядра і, крім того, екрануються від ядра внутрішніми електронами. Внаслідок
цього вплив зовнішнього поля зазнають рівні валентних електронів, порівняно
слабо зв’язаних із ядром.