КОРОЗІЯ
НА КОНТАКТІ ДВОХ РІЗНИХ МЕТАЛІВ
І.
Корозія на контакті ![]() у вологому середовищі в присутності кисню (
у вологому середовищі в присутності кисню (![]() ,
, ![]() ).
Анод – ферум як більш активний метал.
).
Анод – ферум як більш активний метал.
Схема
корозійного гальванічного елемента:
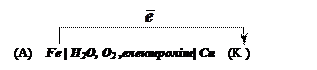
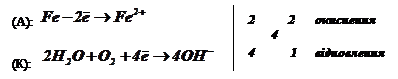 Процеси
на анодній і на катодній ділянках:
Процеси
на анодній і на катодній ділянках:
Сумарне
рівняння процесу корозії:
![]() .
.
Гідроксид
феруму (ІІ) легко окиснюється киснем і водою:
![]() .
.
Утворений
гідроксид феруму (ІІІ) перетворюється у іржу:
іржа
![]()
За
цією схемою відбуваються такі процеси:
-
атмосферна корозія – у вологому повітрі. Швидкість корозії залежить від
вологості повітря, вмісту інших корозійно-активних газів та стану поверхні металу;
-
корозія у природних водах або у водних розчинах. Залежить від рН середовища,
концентрації електролітів, температури;
-
грунтова корозія – це корозія газо-, водо- і нафтогонів, металевих конструкцій,
що знаходяться у вологому ґрунті. Швидкість корозії залежить від вологості
ґрунту. Найшвидше проходить корозія, коли вміст вологи становить 20-25%.
ІІ.
Корозія у воді, що не містить кисню.
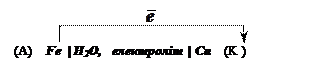 Схема
корозійного гальванічного елемента:
Схема
корозійного гальванічного елемента:
Процеси на анодній і на катодній
ділянках:
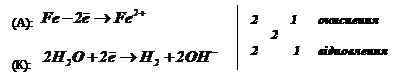
Сумарні
рівняння процесу корозії:
![]() .
.
Процес
корозії іде значно повільніше, бо ![]() без
без ![]() -слабий
окисник.
-слабий
окисник.
ІІІ.
Корозія у кислому середовищі.
Окисник
– іони ![]() .
.
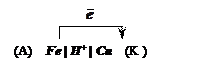 Схема
корозійного гальванічного елемента:
Схема
корозійного гальванічного елемента:
Процеси
на анодній і на катодній ділянках:
(A): ![]()
(K): ![]()
Сумарне
рівняння процесу корозії:
![]()
У
цьому випадку залізо руйнується, утворюючи не іржу, а сіль тої кислоти, яка
створила кисле середовище.
Отже, при контактній електрохімічній корозії
руйнується той метал, потенціал якого менший.

