ЗАЛЕЖНІСТЬ ШВИДКОСТІ ХІМІЧНОЇ РЕАКЦІЇ ВІД ТЕМПЕРАТУРИ
Вплив
температури на підвищення швидкості хімічної реакції пояснює теорія
активації.
Далеко не
кожне зіткнення реагуючих речовин приводить до хімічної взаємодії. Для
утворення нових молекул необхідно ослабити або розірвати зв’язки між атомами і
молекулами реагуючих речовин. При цьому утворюється нестійкий проміжний –
активний комплекс, що характеризується великим запасом енергії. Для його
утворення необхідна надлишкова енергія. Активний комплекс існує дуже короткий
час, він розпадається, виділяючи енергію і утворюючи продукти реакції.
А +
В → А...В
→ А – В
реагуючі активний продукти
речовини комплекс реакції
Надлишкова енергія, яку повинні мати молекули, щоб
їх зіткнення могло привести до утворення нової речовини називається енергією
активації (Еa, кДж/моль). Молекули, енергія яких досягає енергії
активації, називаються активними.
Підвищення температури
збільшує кінетичну енергію і кількість активних молекул, а це приводить до
зростання швидкості хімічної реакції.
Взаємозвязок між температурою, енергією
активації та швидкістю хімічної реакції визначається рівнянням Арреніуса:
![]() ,
,
де ![]() –
константа швидкості;
–
константа швидкості;
![]() –множник
Арреніуса, який оцінює кількість ефективних зіткнень;
–множник
Арреніуса, який оцінює кількість ефективних зіткнень;
![]() – основа натурального логарифма;
– основа натурального логарифма;
![]() – енергія
активації;
– енергія
активації;
![]() – температура.
– температура.
Наближено залежність
швидкості реакції від температури визначають за правилом Вант-Гоффа: при
підвищенні температурі на кожні 10 градусів швидкість більшості гомогенних реакцій збільшується в 2-4 рази.
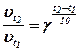 ,
,
де ![]() - швидкості реакції при температурах
- швидкості реакції при температурах ![]() і
і ![]() ;
;
![]() і
і ![]() - кінцева і початкова температури;
- кінцева і початкова температури;
![]() - температурний коефіцієнт швидкості: показує,
у скільки саме разів змінюється швидкість даної реакції при зміні температури
на кожні 10 градусів. Для більшості хімічних реакцій
- температурний коефіцієнт швидкості: показує,
у скільки саме разів змінюється швидкість даної реакції при зміні температури
на кожні 10 градусів. Для більшості хімічних реакцій ![]() .
.

