Т.4 Теорія водневоподібного
атома у квантовій теорії
§1. Принцип
відповідності Бора
Енергія електрона в потенціальній ямі
(бруску провідника) є квантована:
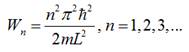
1. Знайдемо “відстань” в одиницях енергії між сусідніми
енергетичними рівнями частинки в потенціальній ямі, зображеній на рисунку 4. 1.
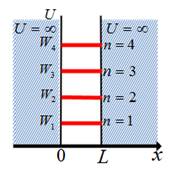
Рис. 4. 1
Енергія частинки на n-ному
енергетичному рівні визначається виразом:
![]()
на n+1
рівні:
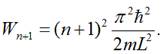
“Відстань” між сусідніми рівнями:
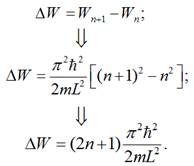
2. Порівняємо, у скільки разів величина енергетичної
щілини між рівнями n і n+1 відрізняється від значення енергії
на n-ному
енергетичному рівні:
Відомо, що:
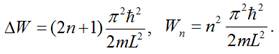
Тоді:
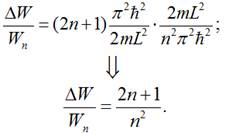
Для
великих значеннях:
![]()
тому:
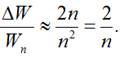
Висновки.
Для більших значень "n"
енергетична щілина ΔW менша за
енергію сусідніх рівнів. Зі збільшенням значення "n" говорити про дискретність енергетичних рівнів з фізичної
точки зору стає неможливим. Таким чином, при збільшенні n класичною стає ситуація з неперервним набором значень енергії
частинки, що рухається.
Принцип відповідності
Бора (1923): для великих квантових чисел висновки і наслідки квантової механіки
повинні приводити до висновків класичної механіки.
§2. лінійний
гармонічний осцилятор
Лінійним гармонічним
осцилятором називається частинка з масою m, яка коливається вздовж осі під дією
квазіпружної сили![]() . Одновимірна модель
руху електрона навколо атомного ядра подібна до лінійного гармонічного
осцилятора, тому його енергія описується у квантових термінах. Зі стаціонарного
рівняння Шредінгера власні значення енергії
гармонічного осцилятора мають такий вигляд:
. Одновимірна модель
руху електрона навколо атомного ядра подібна до лінійного гармонічного
осцилятора, тому його енергія описується у квантових термінах. Зі стаціонарного
рівняння Шредінгера власні значення енергії
гармонічного осцилятора мають такий вигляд:
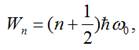
або
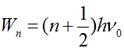 ,
,
тут
![]()
Висновки.
1.
Енергії гармонічних осциляторів кантуються.
2.
Виходячи з вищесказаного, енергії електронів в атомі також повинні бути
виміряні.
3.
Мінімальна енергія, яку може мати гармонічний осцилятор (електрон в атомі),
відмінна від нуля:
![]()
![]()
4. Дана
енергія називається нульовою енергією і не може бути видалена з осцилятора
ніяким охолодженням навіть до абсолютного нуля.
5. Той
факт, що атоми в кристалах зберігають певне "нульове" коливання
навіть при абсолютному нулі, підтверджено дослідами з розсіювання світла
кристалами при різних температурах.
6.
Потенціальна енергія електрона в ядерному полі
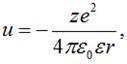
записана
в стаціонарне рівняння Шредінгера
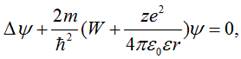
дозволяє з розв’язків цього рівняння
знайти енергію електрона в атомі:
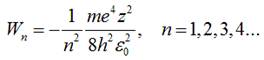
7. Оскільки хвильова функція для електрона в атомі задана в
просторі, то вона має три ступені вільності і, відповідно, характеризується
трьома квантовими числами:
![]()
§3. Квантові числа та їхній фізичний зміст.
Правила відбору.
I. n - це головне
квантове число, яке відповідає не кількісті орбіталей, як у Бора, а кількості
груп станів, в яких два інших квантових числа можуть набувати різних значень:
n=1, 2 ,3, 4
… (правило відбору для n).
II. l - це орбітальне квантове число, яке визначає величину імпульсу
електрона, що рухається навколо ядра:
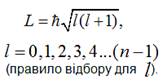
ІІІ. m – це магнітне квантове
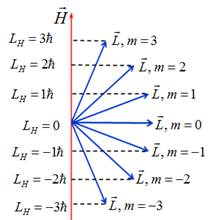
число, що визначає проекцію моменту імпульсу електрона на певний напрям
зовнішнього магнітного поля (див. рис. 4.2):
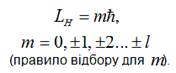
![]()
Рис. 4.2.