7.6. Корозія металів
Корозією зазвичай називають
мимовільне руйнування металів у результаті їхньої хімічної й електрохімічної
взаємодії із зовнішнім середовищем та перетворення їх у стійкі сполуки (оксиди,
гідроксиди, солі).
Власне кажучи, корозія являє собою сукупність окисно-відновних процесів, які відбуваються при контакті металів з агресивним середовищем, що призводить до руйнування металевих виробів. Під агресивним
середовищем мають на увазі окисну атмосферу (присутність
кисню в атмосфері Землі робить її
окисною), особливо в присутності води або розчинів електролітів.
За механізмом процесу розрізняють хімічну та електрохімічну корозію металів. Хімічна корозія являє собою звичайну хімічну реакцію між атомами металів і різних окисників. Прикладами хімічної корозії є високотемпературне окиснення металів киснем, окиснення поверхні алюмінію на повітрі, взаємодія металів із хлором, сіркою, сірководнем H2S тощо.
Електрохімічна корозія протікає
в розчинах, тобто, в
основному, при контакті металів
з розчинами електролітів,
особливо у тих випадках, коли метали перебувають у контакті з менш активними металами. Швидкість корозії істотно залежить від активності
металів, а також від концентрації й природи домішок у воді. У чистій воді метали майже не піддаються корозії, а в контакті з більш активними металами навіть у розчинах електролітів не кородують.
Багато металів, зокрема й Ферум, перебувають у земній корі у вигляді
оксидів. Перехід від металу до
оксиду — енергетично вигідний
процес, інакше кажучи, оксиди більш стійкі сполуки,
ніж метали. Для того щоб
провести зворотний процес і
добути метал з руди, необхідно затратити багато енергії, тому залізо виявляє тенденцію перетворюватися знову в оксид — як кажуть, залізо іржавіє. Іржавіння — це термін для позначення корозії, тобто процесу окиснення металів під дією
навколишнього середовища.
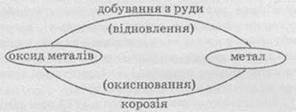
Кругообіг металів у природі
можна зобразити за допомогою такої схеми:
Металеві вироби іржавіють тому, що сталь, з якої вони зроблені, реагує з киснем та
водою, котрі містяться в атмосфері. При корозії заліза або сталі
утворюються гідратовані форми ферум(ІІІ) оксиду різного складу (Fe2О3 ∙ хН2О).
Оксид проникний для повітря
та води й не утворює захисного
шару на поверхні металу. Тож корозія металу
продовжується й під шаром іржі, що утворилася.
Коли метали контактують із вологим повітрям,
вони завжди підлягають корозії, однак на швидкість іржавіння впливає дуже багато
факторів. З-поміж них можна назвати такі:
наявність домішок у металі; присутність кислот або інших електролітів
у розчинах, що стикаються з поверхнею заліза; кисень, який міститься в цих розчинах.