3.2.Каталіз.
Швидкість хімічної реакції змінюється за
наявності деяких речовин. Наприклад, швидкість реакції розкладу хлорату калію
(бертолетової солі) збільшує оксид марганцю (IV) МnО₂:
![]()
Швидкість реакції сполучення алюмінію з йодом
зростає за наявності води:
![]()
Визначення. Речовини, які змінюють швидкість реакції, але не входять до
складу продуктів реакції, називають каталізаторами. Зміна швидкості хімічної реакції за наявності каталізаторів – це
каталіз. Реакції, швидкість яких можна змінити за допомогою каталізаторів,
називають каталітичними.
Кількість каталізатора, що вводять в систему, як
правило, набагато менша за кількість реагуючих речовин. Каталізатор може
змінювати швидкість реакції в багато разів.
Механізм каталізу. Вважається, що каталізатор
утворює з однією з реагуючих речовин проміжну активну нестійку сполуку, яка
розкладається в процесі реакції. Наприклад, реакція між речовинами А і В
протікає повільно. Внаслідок взаємодії каталізатора К з речовиною А утворюється
активна нестійка проміжна сполука АК:
А + К = АК.
Ця сполука легше і швидше взаємодіє з речовиною
В, ніж А з В:
АК + В = АВ + К.
У результаті утворюється речовина АВ і
каталізатор у вільному стані.
Класифікація каталізаторів. Розрізняють кілька
груп каталізаторів.
Специфічні та універсальні каталізатори. Дія
деяких каталізаторів специфічна: каталізатор, який прискорює одну реакцію,
буває зовсім неефективним для іншої. Каталізатор може змінювати не лише швидкість
хімічної реакції, але й її механізм. З однієї речовини, використовуючи різні
каталізатори, можна одержати різні продукти реакції. Наприклад, з етилового
спирту за наявності оксиду алюмінію одержують етилен і воду:
![]()
за
наявності порошку міді – водень і оцтовий альдегід:
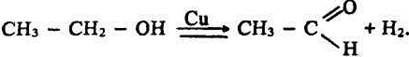
Існують каталізатори з груповою специфічністю. Ці
каталізатори прискорюють однотипні реакції. Наприклад, оксид ванадію (V) V₂![]() прискорює
реакцію окиснення таких речовин, як SO₂, NН₃ та ін.
прискорює
реакцію окиснення таких речовин, як SO₂, NН₃ та ін.
Якщо один і той же каталізатор змінює швидкість
різних реакцій, його називають універсальним. Так, платина як універсальний
каталізатор використовується в багатьох реакціях, наприклад у реакціях оксиду
сірки (IV) з киснем:
![]()
і етилену з воднем:
![]()
Гомогенні та гетерогенні каталізи.
Розрізняють гомогенний та гетерогенний каталізи.
Під час гомогенного каталізу каталізатор знаходиться в тому ж агрегатному
стані, що й реагуюча речовина (газоподібному або рідкому).
У разі гетерогенного каталізу каталізатор
перебуває в іншому агрегатному стані, наприклад каталізатор – тверда речовина,
а реагуючі речовини – гази.
Під час гетерогенного каталізу реакції
відбуваються на поверхні каталізатора, тому їх швидкість залежить від площі та
властивостей поверхні. Каталізатор абсорбує молекули реагуючих сполук і
збільшує їх активність.
Каталітичні отрути. Речовини, які зменшують або
пригнічують активність каталізаторів, називають каталітичними отрутами.
Каталітичні отрути утворюють з каталізаторами малоактивні або нереакційноздатні
сполуки.
Застосування каталізу. Каталіз широко
використовують у багатьох технологічних процесах, особливо в хімічній промисловості
(у виробництві аміаку, азотної та сірчаної кислот, органічному синтезі).
Швидкість багатьох хімічних реакцій, що
відбуваються в живих організмах, регулюється біологічними
каталізаторами ферментами (особливо білковими молекулами).