Розділ
8. Корозія будівельних матеріалів і
захист від неї
Люба будівельна споруда в процесі служби знаходиться в контакті з навколишнім середовищем. Як наслідок, матеріал з якого виконані будівельні конструкції, протягом всього терміну експлуатації взаємодіє з компонентами цього середовища. В багатьох випадках можлива хімічна взаємодія матеріалу конструкцій і середовища. Якщо така
взаємодія приводить до зниження
властивостей міцності матеріалу — до його часткового чи повного
руйнування, говорять про «агресивність» середовища по відношенню до даного матеріалу.
Інтенсивність взаємодії
матеріалу і середовища залежить від фізичних
умов: температури, фазового складу агресивного середовища, умов
контакту, наявності тиску рідкого чи газоподібного
середовища, швидкість його руху біля
поверхні споруд і інших факторів. Хімічні і фізико-хімічні процеси,
за якихруйнується матеріал,
називають процесами корозії.
При проектуванні в будівництві споруд різного призначення необхідно передбачити можливість розвитку корозійних процесів і їх наслідки.
Стійкість і довговічність споруд в значній мірі залежить від відповідності властивостей
матеріалу, з якого виконана споруда і її окремі конструктивні
елементи, умовам її роботи, тому розуміння корозійних процесів І своєчасне попередження їх розвитку є важливою умовою сучасного будівництва довговічних споруд.
Основні будівельні конструкційні матеріали, як традиційні (дерево, сталь, бетон і залізобетон),
такі нові (склопластики, полімербетони, полімерні плівки, алюміній і його сплави), здатні хімічно взаємодіяти з
компонентами газоповітряного
середовища, з водою і розчиненими
в ній речовинами. Процеси корозії будівельних матеріалів відбуваються у водному середовищі.
З хімічної точки зору це реакції нейтралізації
чи обміну, в яких приймають участь компоненти, що складають матеріал і речовини, розчинні у воді. Як правило, в природних
водах розчинені солі, а в промислових рідких середовищах різні сполуки: від кислот і
лугів до складних органічних сполук. В загальному вигляді реакції, що визначають корозійний процес, схематично можуть бути записані рівняннями: А + В <-> С + Д і А + В <-> АВ. Напрямок корозійного процесу буде визначатись властивостями реагуючих речовин і продуктів реакції Якщо в результаті взаємодії компонентів утворюється нерозчинна чи важкорозчинна
речовина, то процес буде йти в бік утворення
таких продуктів. Місце виділення і властивості речовин, які утворюються
в процесі корозії, визначають інтенсивність багатьох корозійних процесів. Аналогічно впливає на напрямок корозійного процесу і видалення одного з продуктів реакціїз розчину у вигляді газу.
Корозійні
процеси відбуваються з різною швидкістю. Як правило, напрямок і кінцевий
результат реальних корозійних процесів визначається кінетичними факторами.
Стійкість
різних будівельних матеріалів до агресивних дій зовнішнього середовища
визначається перш за все їх хімічним складом і реакційною здатністю. Різниця в
хімічній природі будівельних матеріалів зумовлює різні умови для їх стійкості
при дії зовнішнього середовища. В той же час як сталь, наприклад, не є стійкою
до дії кисню повітря у вологій атмосфері, бетон в таких умовах збільшує свою
міцність. Матеріали на основі полімерів стійкі, хоча і в різному ступені, до
дії хімічних реагентів — кислот, лугів, солей, але піддаються деструкції на
світлі в результаті дії ультрафіолетового випромінювання. Для натуральних
камінних матеріалів така дія несуттєва. Приклади можна було б продовжити. Далі
детально розглянемо окремі корозійні процеси на прикладі цементного бетону як
основного сучасного конструктивного матеріалу.
Розглянемо
спочатку процеси корозії неорганічних будівельних матеріалів— натуральних
камінних матеріалів, будівельної кераміки, бетонів.
Ці
матеріали об'єднує спільність їх структури: всі вони капілярно-пористі тіла.
Але між ними є і суттєві відмінності. Натуральні камінні матеріали, вірніше
частина з них — вивержені породи — хімічно досить інертні і мають низьке
значення пористості. Осадкові карбонатні породи, які складаються з вапняку —
вуглекислого кальцію, чи доломіту— подвійної вуглекислої солі кальцію і магнію
(СаСОз* МgСОз),
як правило, мають більш високу відкриту пористість, ніж вивержені, і, як це
видно з їх хімічного складу, будуть нестійкі до дії кислот. Кераміка хімічно високостійка, але її пористість може змінюватись в широких
межах — від десятих часток відсотка до 10 —20%; тому процеси, за яких речовина
накопичується в порах матеріалу чи в ході яких можливе заморожування і
відтаювання водних розчинів, що насичують матеріал, можуть руйнувати кераміку.
З неорганічних конструкційних матеріалів найбільш хімічно активний цементний
камінь бетону, який характеризується високою (до 30% об'єму) пористістю.
Правда,
ця пористість досить високодисперсна, що підвищує опір бетону прониканню в його
об’єм агресивних компонентів зовнішнього середовища.
Хімічна активність і пористість
цементного каменю зумовлюють і особливості корозійних процесів при дії на нього
зовнішнього середовища.
В. М. Москвин
запропонував класифікувати основні корозійні процеси при дії рідких агресивних
середовищ на цементний камінь чи бетон на три види. До першого виду корозії
відносяться процеси, при яких у воді, що фільтрується через бетон чи, що омиває
споруду, розчиняються складові частини цементного каменю, перш за все гідрат
оксиду кальцію (Са(ОН)2), до другого виду
належать корозійні процеси, що складаються з реакцій обміну між компонентами
середовища і цементного каменю з утворенням розчинних у воді продуктів, які
можуть бути винесеними з структури, чи рихлих, що не мають в’яжучих
властивостей продуктів, які залишаються в ній; до третього виду — процеси, в
яких основним руйнівним фактором єнакопичувані в
порах, тріщинах і
капілярах бетону солі, які в певних умовах можуть руйнувати бетон.
В усіх випадках вирішальне
значення має швидкість корозійного процесу, яка в умовах гетерогенних реакцій,
що відбуваються на поверхні розділу твердої та рідкої фаз і при відсутності
гідростатичного тиску, буде лімітуватись швидкістю дифузії агресивних
компонентів в глибину цементного каменю чи гідрату оксиду кальцію назустріч
агресивному компоненту. Кількість речовини, яка переноситься за рахунок дифузії
пропорційна різниці концентрацій на початку і в кінці шляху дифузії. А тому
можна вважати, що інтенсивність корозійного процесу пропорційна концентрації
агресивного компонента в водному середовищі. Звідси напрошується висновок про
порівняльну шкідливість дії агресивного середовища залежно від його концентрації. Таке
співставлення може бути корисним при розв’язанні питання про допустимі межі
вмісту агресивного компонента залежно від терміну служби споруди.
Агресивна дія значно посилюється,
якщо вода діє на бетонну конструкцію під тиском. В даному випадку навіть при
невеликих тисках ( десяті частини метра водяного стовпа) кількість розчиненої
агресивної речовини, яка поступає в структуру цементного каменю бетону, значно
перевищує ті кількості, які можуть проникнути в тих же умовах, тільки внаслідок
дифузії. Тому корозійні процеси в спорудах, що знаходяться під тиском, стають
інтенсивнішими. При проектуванні споруд і їх введенні в експлуатацію важливим
завданням є надання будівельним конструкціям надійної стійкості протягом
певного часу. Розглянемо ступені небезпечності окремих хімічних взаємодій.
Загальновідома розчинна здатність води. В природі
безперервно відбуваються процеси розчинення гірських порід і утворення нових.
Особливо інтенсивно розчиняються карбонатні породи.
Широко розповсюджені карстові явища — утворення в земній корі, в районах, які
складаються з вапняків і доломітів, великих пустот — печер — що є наслідком
процесів розчинення цих порід водою і водою, що містить розчинену вуглекислоту.
Аналогічний процес може
відбуватись і з бетоном. Як відомо, розчинність Са(ОН)2
складає 1,3 г/л води (в розрахунку на СаО). Але така
концентрація може бути досягнута тільки за повільної фільтрації води через
товщу бетонної конструкції.
Розглянемо механізм руйнування
бетону при вилудженні. У випадку, якщо вода омиває
бетонні споруди, швидкість руйнування бетону буде залежати від швидкості
дифузії гідроксиду кальцію з глибини бетону до його зовнішньої поверхні, що
контактує з водою. В першу чергу з поверхневого шару буде розчинятись гідроксид
кальцію, який виділився при гідролізі трьохкальцієвого
силікату. Потім буде йти гідроліз гідросилікатів і гідроалюмінатів
кальцію, оскільки ці сполуки стійкі в контакті з водою тільки при вмісті в ній
розчиненого і певної для кожної сполуки кількості гідроксиду кальцію, тобто за
наявності рівноважної концентрації гідроксиду кальцію. На поверхні бетону при
цьому створюється шар продуктів корозії цементного каменю. Якщо ці продукти
зберігаються на місці, наприклад на бетонних фундаментах, які знаходяться в
ґрунті чи в резервуарах, які працюють при постійному заповненні водою,
швидкість корозії з часом швидко зменшується внаслідок росту дифузійного опору
шару продуктів корозії.
Кількість розчиненого гідроксиду
кальцію в даному випадку пропорційна кореню квадратному з часу від початку
процесу. Якщо продукти корозії видаляються з поверхні, наприклад при великій
швидкості руху води чи при механічній дії наносів, швидкість корозії буде
постійна і буде визначатись тільки постійною швидкістю дифузії гідроксиду
кальцію через «активний», що бере участь в дифузійному процесі шар, що не
втратив міцності.
Найбільш небезпечні розчинення і
винесення вапна для бетонних і залізобетонних, а особливо тонкостінних,
конструкцій під натисковою
дією води. При постійній фільтрації води з бетону буде виноситись вапно в
кількості, що пропорційна кількості профільтрованої води ( в перерахунку на
одиницю об’єму бетону) і середній концентрації вапна в цій воді.
Можна вирахувати кількість води,
яка повинна фільтруватись через дану конструкцію, щоб вивести кількість вапна,
виведення якої може зумовити зменшення міцності, що перевищує допустиму.
Дослідження показали, що видалення 20% гідроксиду кальцію від загального
початкового вмісту в портландцементі приводить до катастрофічного падіння
міцності цементного каменю, оскільки при цьому послаблюються не тільки
контакти, що створені кристалами вапна, але і починається процес розкладу —
гідроліз гідросилікатів кальцію — основної складової каркасу міцності
цементного каменю. Причому розчинення починається з найбільш напружених і
відповідальних ділянок структури.
В практиці корозії бетону внаслідок
розчинення вапна (корозія першого виду) має місце при дії «м’яких» вод на
бетон. До м’яких відносяться води снігові, дощові і інші, що не містять значної
кількості розчинених солей кальцію і магнію. Це умовна назва, але вона
характеризує властивості природної води, що використовується для побутових
потреб. В м’якій воді краще піниться мило, вона не дає накипу в посуді.
Звичайно природні води, протікаючи під землею чи по її поверхні, розчиняють
деяку кількість солей кальцію і магнію, перш за все у вигляді двовуглекислих
солей Са(НСО3)2 і Мg(НСО3)2.
Це відбувається тому, що вода при контакті з повітрям розчиняє рівноважну
кількість вуглекислоти з повітря, а вуглекислота реагує з карбонатними породами
і переводить їх в розчин:
СаСО3 +СО2
+ Н2О = Са(НСО3)2;
МgСО3+СО2 +
Н2О = Мg(НСО3)2.
Корозія першого виду, як вже було
сказано, небезпечна для споруд, на які вода діє під натиском і може
фільтруватись через бетон (мал. 10). Якщо споруда
знаходиться в ґрунті, небезпека розчинення бетону досить невелика, оскільки
продукти корозії поверхневого шару бетону — нерозчинні гелі кремнієвої кислоти
і інші сполуки — залишаються на місці і створюють шар, який перешкоджає
подальшій дифузії гідроксиду кальцію з цементного каменю, тобто процес корозії
в даному випадку сповільнюється.
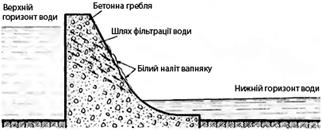
Мал. 10.
Розчинення і винесення гідроксиду кальцію з бетону
Цементний камінь бетону має лужну
реакцію, тому він найбільш активно реагує з кислотами. Практично всі кислоти,
що взаємодіють з гідроксидом кальцію, а потім і з гідросилікатами і гідроалюмінатами кальцію, зумовлюють інтенсивне руйнування
цементного каменю і бетону.
При дії кислоти на гідроксид
кальцію цементного каменю утворюються солі — це реакція нейтралізації, і в
залежності від властивостей кальцієвих солей різних кислот агресивна дія
останніх буде різною. Якщо утворюються важкорозчинні солі, то вони випадають в
порах цементного каменю і створюють перепону для розвитку корозійного процесу,
якщо солі легкорозчинні, процес буде відбуватись інтенсивно.
Так, кремнійфтористоводнева кислота взаємодіє з
гідроксидом кальцію за схемою:
Н2ЅіF4 +
3Са(ОН)2 = ЅіО2 + 3СаF2 + 4Н2О.
Утворені фтористий кальцій і гель
двоокису кремнію — сполуки важкорозчинні. Тому навіть при порівняно високих
концентраціях дія цієї кислоти носить затухаючий характер. В той же час соляна чи оцтова кислоти, солі яких добре
розчинні у воді, сильно агресивні по відношенню до бетону.
Останнім часом розроблена
кількісна теорія дії кислот на бетон і запропоновані розрахункові формули для
оцінки швидкості процесів кислотної корозії. З достатньою для практичних цілей
точністю процес кислотної корозії бетону описується рівнянням L =А![]() , де L—
глибина руйнування бетону;
, де L—
глибина руйнування бетону; ![]() — час дії кислоти; А — коефіцієнт, що враховує
вид і концентрацію кислоти, властивості бетону і умови взаємодії кислоти і
бетону.
— час дії кислоти; А — коефіцієнт, що враховує
вид і концентрацію кислоти, властивості бетону і умови взаємодії кислоти і
бетону.
Найбільш поширена в природі
вуглекислота — вона діє на бетон у всіх споруд, які знаходяться на повітрі і в
воді. Вуглекислота, що розчинена у воді, взаємодіє з гідроксидом кальцію
(мал.11,а) і утворює вуглекислий кальцій (мал.11,б). При великих концентраціях
вуглекислоти вона може діяти і на вуглекислий кальцій з утворенням
двовуглекислого кальцію (мал. 11,в) в системі, яка
складається з СаСО3, СО2, Са(НСО3)2,
створюється рухлива рівновага:
СаСО3 + СО2
+Н2О ↔ Са(НСО3)2.
Як тільки змінюється концентрація
вуглекислоти, зміщується рівновага. Агресивним по відношенню до бетону є тільки
надлишкова в порівнянні з рівноважною кількість вуглекислоти. Як наслідок, у
водах з високою тимчасовою твердістю, тобто з високим вмістом двохвуглекислого кальцію Са(НСО3)2,
може бути присутня велика кількість вільної вуглекислоти, що не є небезпечною
для бетону. Розрахувати цю кількість можна на основі даних про рівновагу в цій
реакції чи за емпіричними даними.
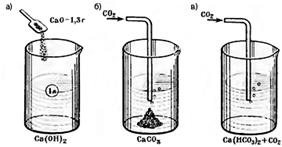
Мал. 11. Дія
вуглекислого газу на розчин гідроксиду кальцію
Крім вуглекислоти, в природних болотних водах зустрічаються
вільні гумінові кислоти. Це малодисоційовані кислоти,
що утворюють важкорозчинні кальцієві солі, тому їх агресивність невелика.
Взагалі щільні бетони гарантують стійкість залізобетонних споруд в болотних
водах. Багатогранні хімічні процеси відбуваються при дії на бетон розчинів солей. Природні води
і промислові рідини, агресивні по відношенню до бетону, містять різні солі.
Деякі з них не вступають в реакції взаємодії з мінералами цементного каменю,
інші взаємодіють досить активно. До першої групи відносяться, наприклад, досить
розповсюджені в природі хлориди, перш за все хлорид натрію.
Хлорид натрію в присутності
надлишку гідроксиду кальцію повільно реагує з алюмінатними
мінералами цементного каменю з утворенням гідрохлоралюмінату
кальцію. Розчини хлористих солей небезпечні для залізобетонних конструкцій
тільки у випадку можливої дії їх в умовах почергового насичення і висушування
чи капілярного підсосу. В умовах періодичного насичення розчином і
висушування розчин мігрує в поровому просторі цементного каменю; при цьому можуть
послаблюватись контакти з-за підвищеної розчинності гідроксиду кальцію в
присутності хлориду натрію. При
капілярному підсосі в порах бетону біля поверхні випаровування накопичуються
солі. Якщо випаровування є досить інтенсивне, то фронт випаровування розміщується в глибині бетону на деякій
відстані від його поверхні, де і виділяються кристали солі. Заповнення пор
кристалами солі може привести до розвитку кристалізаційного тиску і відповідно
руйнування бетону.
Аналогічно діють і розчини інших
розчинних солей, що не реагують з цементним каменем.
Значно більш небезпечні для бетону води, що містять сульфати. При цьому виді
агресивної дії бетон розбухає, на конструкціях появляються тріщини. Такий
характер руйнування зумовлений тим, що при взаємодії сульфатів з цементним каменем хімічна реакція відбувається з утворенням складних
комплексних сполук — гідросульфоалюмінатів
кальцію. При утворенні гідросульфоалюмінатів
зв’язується значна кількість води:
3СаО*АІ2О3 + 3СаЅО4 +
30Н2О = 3СаО*АІ2О3*3СаЅО4*30Н2О.
Розрахунок за відносними молекулярними масами і густиною реагуючих речовин
дозволяє визначити зміну об’єму
мінералів цементного каменю при їх переході в новоутворення. При реакції
утворення трьохсульфатної форми гідросульфоалюмінату
кальцію об’єм твердої фази збільшується в
2,6 рази (мал. 12).
Агресивна дія сульфатних розчинів
залежить від концентрації сульфат-йона в розчині, а
також від мінералогічного складу цементного клінкеру. Чим вищий вміст алюмінатної фази в цементному камені,
тим менш стійкий бетон на даному цементі.
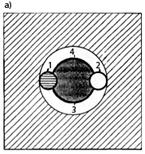
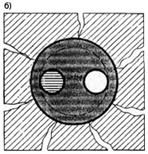
Мал. 12.
Умовне співвідношення об’ємів компонентів до сульфатної корозії бетону (а) і
після неї (б)
1 —3СаО *АІ2
О3, що прореагував з гіпсом; 2 — СаЅО4;
3 —3СаО *АІ2О3 *3СаЅО4*30Н2О;
4 — пори
Сульфатостійкість суттєво
підвищується, якщо застосовується цемент з низьким вмістом трьохкальцієвого
алюмінату. Відомо, що для підвищення сульфатостійкості
цементного каменю випускається спеціальний, сульфатостійкий цемент, що містить
в клінкері обмежену (не більше 5%) кількість трьохкальцієвого
алюмінату. Руйнування при дії сульфатного розчину відбувається звичайно
повільно, оскільки швидкість процесу визначається дифузійним проникненням
сульфатів в глибину бетону. Процес цей спочатку гальмується внаслідок
ущільнення порової структури цементного каменю, але
потім починає йти з прискоренням внаслідок появи тріщин,
які збільшують проникнення агресивного розчину в бетон. Тут ми маємо
приклад сполучення хімічних та фізичних процесів, які одночасно руйнують
цементний камінь. Такі процеси відносяться до третього виду корозії за
класифікацією В.М.Москвіна.
Одним з складних випадків
корозійного руйнування бетону є дія на нього морської води. Вміст солей у воді
різних морів є різним. Якщо в океані він досягає 35 г/л, то в Чорному морі —
близько 18 г/л, в Каспійському —14 г/л, в Балтійському — 8 -12 г/л. Але співвідношення окремих солей
змінюється незначно. Більше всього в морській воді хлористого натрію. Вміст
сульфатів в перерахунку на йон ЅО42-
складає в океанській воді близько 2,7 г/л. Але обстеження бетонних і
залізобетонних споруд, які довгий час піддавались дії морської води, показали,
що в бетоні (в його порах, тріщинах, дефектах)
накопичується біла маса. Хімічні аналізи показали, що гідрооксиду магнію.
Магній в морській воді міститься переважно у виді сірчанокислої солі. Взаємодія
сірчанокислого магнію з гідратом оксиду кальцію цементного каменю — необоротна
реакція з утворенням практично нерозчинного гідрооксиду магнію:
МgЅО4 + Са(ОН)2 = Мg(ОН)2
↓ + СаЅО4.
Точно так же, як і сульфат
магнію, реагує люба розчинна сіль магнію, тобто при дії сполук
магнію відбуваються процеси по механізму корозії другого виду. Бетон можуть руйнувати не тільки вода і водні
розчини. Навіть повітря викликає процеси, які відображаються на міцності
залізобетону. А тому поведінка бетону і стальної арматури при їх взаємодії з
складовими частинами повітря зовсім різне. Ми розглянемо дію повітря лише на
бетон. Азот, кисень, інертні гази, що входять до складу повітря, практично не
діють на цементний камінь в бетоні. Лише вуглекислий газ, який міститься в
повітрі в кількості 0,03%, помітно впливає на бетон. Розчиняючись у воді, він
утворює вуглекислоту, про дію якої говорилось раніше. При тривалій дії
вуглекислоти повітря в поверхневому шарі бетону гідроксид кальцію
нейтралізується за відомою уже реакцією:
Са(ОН)2 + СО2
= СаСО3↓ +Н2О.
При цьому відбувається деяке
ущільнення бетону, яке неважко підрахувати, знаючи густину кожної з реагуючих сполук і використовуючи їх стехіометричні
співвідношення по цій реакції. Підрахунок показує, що об’єм твердої фази при
взаємодії вапна і вуглекислоти збільшується на 11% (мал.
13,а,б). Ущільнення поверхневого шару в результаті дії вуглекислоти позитивно
впливає на стійкість бетону в конструкціях.
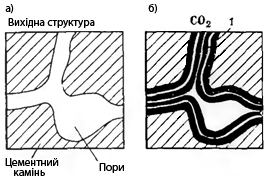
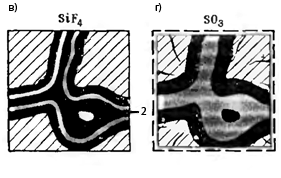
Мал.13. Ущільнення цементного
каменю при дії різних газів
1 —об’єм заповнений продуктами
реакції газу з вільним Са(ОН)2;
2 — об’єм заповнений в результаті
взаємодії газу з гідратованими
новоутвореннями
Коли використовували бетони
порівняно малої густини, карбонатизація могла суттєво підвищити стійкість
бетону до дії агресивного середовища. Наприклад, бетонні масиви для морських споруд спеціально
витримували на повітрі перед опусканням в морську воду. Щільні бетони піддаються дуже повільній карбонатизації, і
використання цього процесу для надання стійкості залізобетонним конструкціям
стає малоефективним.
Глибину переродження бетону в
результаті дії вуглекислоти повітря можна виявити за допомогою індикаторів —
речовин, які змінюють свій колір залежно
від реакції середовища, тобто від концентрації в ній водневих йонів. В кислому середовищі вони мають одне забарвлення, в
лужному — інше. Існують речовини, які змінюють колір декілька разів при
поступовій зміні реакції середовища — при різних значеннях рН.
Для визначення лужності цементного каменю застосовують фенолфталеїн,
що змінює колір при водневому показнику рН близько 8.
В розчині Са(ОН)2 фенолфталеїн має
малинове забарвлення, а в нейтральному і кислому середовищах з рН менше 8 він безбарвний. Якщо свіжий злом бетону чи
розчину змочити декількома краплинами розчину фенолфталеїну, то ділянки
цементного каменю, що містять вільний гідроксид кальцію, забарвляться в
малиновий колір, а ділянки, на яких відбулась карбонізація залишаться
безбарвними.
Від ходу карбонізації у великій
мірі залежить довговічність тонкостінних залізобетонних конструкцій. У випадку,
коли карбонізація захопить весь захисний шар бетону і розповсюдиться до
арматури, бетон втратить свої захисні властивості по відношенню до сталі і
стане можлива корозія арматури у вологому повітрі. За малої розчинності солей
відбувається ущільнення бетону чи цементного каменю в об’ємі газами, що
утворюють нерозчинні сполуки з цементним каменем,
може бути проілюстровано на прикладі реакції між чотирьох фтористим кремнієм і
гідроксидом кальцію з утворенням нерозчинного стійкого фтористого кальцію і
кремнезему:
ЅіF4 + 2Са(ОН)2 = 2СаF2 + Н2О + ЅіО2.
Така обробка називається ократирування.
По суті ократирування
схоже з флюатируванням — обробкою поверхні бетону
водними розчинами кремнефтористоводневої кислоти. При
правильно підібраній рецептурі кислота не тільки не руйнує бетон, але створює
на його поверхні захисний шар, який підвищує стійкість бетону до дії агресивних
середовищ.
Фтористі сполуки (мал. 13,в) застосовуються для надання стійкості бетону,
мають дуже цікаві властивості, оскільки дають газоподібні чи розчинні сполуки з кремнієм, які в лужному
середовищі цементного каменю легко переходять в нерозчинні сполуки. Утворення
нерозчинних сполук лежить в основі всіх методів
хімічної обробки бетонів з метою підвищення його стійкості.
Інші газоподібні речовини в
присутності води будуть діяти на бетон у відповідністю зі своєю природою.
Сірчистий ангідрид (ЅО2), розчиняючись у воді, утворює сірчисту
кислоту, яка, як і люба інша кислота, буде взаємодіяти з гідроксидом кальцію в
порах цементного каменю з утворенням відповідної солі, в даному випадку
сірчанокислого кальцію. При цьому можливе окислення сірчистої кислоти і її
солей до сульфатної кислоти і її солей, наприклад гіпсу, і як наслідок —
розвиток в подальшому сульфатної корозії. Інші кислотні гази — сірководень,
сірчаний ангідрид, хлороводень і інші —братимуть участь в реакціях нейтралізації
з гідроксидом кальцію. Їх ступінь агресивності визначається розчинністю
утворених солей.
Нейтралізація з поверхні бетону,
тобто створення на ній плівки нерозчинних стійких сполук,
необхідна, наприклад, для покращення щеплення поверхні з лакофарбовими
покриттями. Поверхня може бути нейтралізована або фтористоводневою кислотою, чи
іншими кислотами, що утворюють нерозчинні сполуки з гідроксидом кальцію: щавелевою, фосфатною.
Ці приклади показують, що
реакції, які викликають руйнування бетону, можуть в певних умовах приводити до
підвищення його стійкості внаслідок утворення важкорозчинних продуктів. За
останні роки вивчено дію на бетон багатьох сполук, а
особливо органічних. Було доведено, що процеси корозії в цьому випадку можуть
бути класифіковані на основі тих же принципів, які враховувались при взаємодії
цементного каменю і неорганічних сполук. При
гідролізі органічних речовин у водному розчині, наприклад, деяких хлорпохідних
продуктів , що використовуються при виробництві синтетичних каучуків,
у водний розчин виділяється хлористий водень, який діє по механізму корозії
другого виду. Деякі органічні продукти здатні до полімеризації в присутності
лугу (наприклад, мономер хлоропрен). В процесі полімеризації збільшується об’єм
матеріалу, що створює внутрішній тиск в структурі бетону, і руйнування
відбувається аналогічно процесам корозії третього виду.
Ще недавно здавалось, що питання
корозії бетону вивчено досконало і, якщо притримуватись простих хімічних
уявлень, можна ясно класифікувати корозійні дії і оцінити ступінь агресивності
того чи іншого зовнішнього середовища. але наприкінці 30-их років вчені
звернули на те, що в деяких районах США бетон багатьох споруд (цементобетонні
покриття доріг, опори мостів, гідротехнічних споруд) через
декілька років після їх
будівництва починає руйнуватись. На поверхні конструкцій появляються тріщини, бетон
набухає. З тріщин виділяється біла речовина. Ніяких
агресивних речовин в зовнішньому середовищі не було. На споруди в процесі
експлуатації попадала тільки дощова вода. Вивчення зразків бетону і матеріалів,
які були застосовані, дало неждані результати. Виявилось, що руйнування
відбувається у всіх випадках, коли для бетону були застосовані гірські породи,
що містять аморфний кремнезем у вигляді опалу. Причому процес відбувається лише
в бетонах, цементи яких містили підвищену кількість сполук
лужних металів — натрію і калію.
В цементі таких сполук міститься невелика кількість (до 1%). Лужні метали
присутні в цементному клінкері в вигляді сполук
типу гідросилікатів кальцію, в яких
частина кальцію замінена натрієм чи
калієм чи у вигляді сульфатів. При гідратації цементу лужні сполуки піддаються
гідролізу в першу чергу і утворюють в водному розчині гідрооксиди NаОН і КОН.
Сірчанокислі солі також легко розчиняються у воді, що заповнює міжпоровий простір в цементному камені.
При контакті такого розчину з аморфним
кремнеземом, що легко піддається дії лугів, вони обов’язково взаємодіють з
утворенням гідросилікатів натрію, загальною формулою nNа2О* mЅіО2*аq. Механізм корозійного процесу при цьому повністю не
вивчений, але можна передбачити, що важливу роль в подальшому відіграють
процеси осмосу, що повільно розвиваються, через плівки, що виникають в
результаті дифузії гідросилікату натрію в цементному камені
з утворенням мембран із гідросилікатів кальцію. Внутрішній тиск, який
розвивається в мікроосмотичних ячейках,
приводить до руйнування цементного каменю. В залежності від кількості активного
кремнезему в заповнювачі і розміру його зерен, процес відбувається з більшою чи меншою швидкістю і
інтенсивністю.
Аналогічні руйнування були
виявлені і в Європі на Атлантичному побережжі в Данії. Породи, що містять
активний кремнезем, є і на території України. В цементній промисловості
намітилась тенденція повного вловлювання і повертання в технологічний цикл
пилу, що виділяється при випалюванні клінкеру, що приводить до збільшення
вмісту в цементі лугів. Розширення виробництва цементу з підвищеним вмістом
лугів, використання в якості заповнювачів порід, що містять аморфний кремнезем,
і випуск бездобавочних цементів можуть привести до
більш широкого розповсюдження «лужної» корозії на наших будівництвах. Це можна
уникнути, нормуючи вимоги до хімічного і мінерального складу цементів і
заповнювачів з тим, щоб виключити умови для розвитку такої корозії. Небезпеку
лужної корозії слід мати на увазі і при використанні солей лужних металів в
якості добавок до бетонів при виконанні робіт в зимових умовах чи для іншої
мети.
Основну увагу ми приділили
корозії бетонуі бетонних і залізобетонних
конструкцій. Це не випадково. З неорганічних будівельних матеріалів це найбільш
розповсюджений і в той же час один з самих чутливих до хімічної дії зовнішнього
середовища матеріал. Натуральні камінні матеріали входять до складу бетону як
основна його складова частина по масі. Вони більш стійкі, ніж штучний цементний
камінь, і беруть участь в роботі бетону, тому про їх стійкість можна судити по
стійкості бетону.
Хімічна стійкість кераміки також
значно вища, ніж цементні матеріали. В будівництві все більше використання
знаходять полімерні матеріали. Це, як правило, значно більш хімічно стійкі
матеріали, ніж цементні бетони.
Таким чином, питання корозії і
захисту від неї будівельних матеріалів представляють собою часто складний
комплекс хімічних (фізико-хімічних) і фізичних процесів, причому рішення цих
питань вдається знайти тільки при врахуванні тих і інших. Нерідко корозія
будівельних матеріалів носить переважно хімічний характер, але і в тих
випадках, коли корозійні процеси в будівельних матеріалах (наприклад, таких, як
руйнування конструкцій в результаті кристалізації в порах матеріалу солей) в великій мірі
залежить від протікання фізичних процесів, неврахування хімічних аспектів
корозії звичайно не забезпечує оптимального захисту.
Особливо суттєва при цьому та
обставина, що корозія будівельних матеріалів — один з найбільш розповсюджених
процесів, що приводять до пониження довговічності конструкцій. Тому
інженеру-будівельнику необхідно рахуватись з цим при проектуванні конструкцій і
споруд і виборі засобів і методів
захисту їх від корозії.
Запитання для самоконтролю:
1. Від яких
факторів залежить корозія будівельних матеріалів?
2. Назвіть
відомі Вам способи захисту від корозії будівельних матеріалів.
3. Що являє собою процес ократирування?
4. Який
вплив органічних сполук на корозію бетону?