Тема 8. Фізіологія збудливих тканин
1.
Мембранний потенціал спокою
2.
Потенціал дії
3.
Механізм проведення збудження нервовими волокнами
4.
Посмуговані м'язи
5.
Механізм м'язового скорочення
6.
Особливості гладких м'язів
7.
Міжклітинна передача збудження і гальмування
Основною
властивістю живих систем є здатність відповідати на вплив навколишнього
середовища активною реакцією. Особливо яскраво ця властивість виявляється в
реакціях нервової, м'язової і залозистої тканин, які називають збудливими, тобто здатними відповідати збудженням
на вплив подразників. Подразнення зумовлює у клітині складний комплекс мікроструктурних перебудов, а також зміни обміну речовин,
концентрації й швидкості руху іонів та їх розподілу на клітинних мембранах.
Жива клітина при
здійсненні своїх функцій безперервно генерує і підтримує електричні потенціали.
Основними іонами, які беруть участь у генерації електричних потенціалів клітин,
є К+, Na+ i
Сl–. За умовами
виникнення в живих структурах розрізняють мембранні потенціали спокою (МПС)
та потенціали дії (ПД).
1.
Мембранний потенціал спокою
У всіх клітинах
поверхневий шар цитоплазми є спеціалізованою структурою, яка називається клітинною
мембраною (оболонкою, цитолемою). Ця мембрана електрично поляризована, і різницю
потенціалів між зовнішньою і внутрішньою пластинками (поверхнями) клітинної
мембрани називають мембранним потенціалом спокою (МПС).
Мембрана – це
тонкий (завтовшки 5-10 нм) утвір, який складається з ліпідів, білків і
мукополісахаридів. Бімолекулярний шар ліпідів є матриксом (каркасом) мембрани,
в який занурені білкові молекули, що утворюють канали для води і іонів,
формують іонні насоси. Мукополісахариди,
розміщені у вигляді "дерев" на поверхні клітинної мембрани,
здійснюють рецептивні функції. Мембрана постійно оновлюється, і її властивості
можуть дещо змінюватися.
Існування МПС
зумовлене: 1) нерівномірною концентрацією іонів у поза- та внутрішньоклітинному
просторі; 2) різна проникність клітинної мембрани для різних іонів. Клітинна
мембрана легко проникна для жиророзчинних речовин, молекули яких проходять
крізь її ліпідний матрикс. Водорозчинні молекули
великого діаметра, у тому числі й аніони органічних кислот, практично не
проникають крізь мембрану. У стані фізіологічного спокою клітинна мембрана є
проникною для К+, оскільки в ній є спеціальні калієві канали, що
пропускають лише гідратований калій.
Коли К+
виходить з клітини, він затримується на зовнішній поверхні клітинної мембрани,
створюючи її позитивний заряд. Великі аніони не можуть пройти з клітини крізь
мембрану і накопичуються біля її внутрішньої поверхні, створюючи негативний
потенціал. Так виникає трансмембранна різниця потенціалів, або МПС.
Цей потенціал
протидіє подальшому виходу К+ за електрохімічним градієнтом.
У стані спокою
клітинна мембрана є добре проникною не лише для К+, вона певною
мірою проникна також для інших іонів, зокрема Na+, C1–, Са2+.
Потоки цих іонів порушують рівноважний стан. Той факт, що в умовах спокою Na+ постійно надходить у клітину, а К+ виходить з
неї, має дуже важливі наслідки, оскільки система не може бути фактично
врівноважена за допомогою звичайної дифузії і простого відновлення заряду на
клітинній мембрані. Якщо немає інших процесів, то клітина дуже швидко
накопичуватиме Na+ і втрачатиме К+ що зменшить їх
трансмембранний градієнт. Отже, цей процес може призвести до різкого зниження
МПС і загибелі клітини. Проте такого не відбувається, оскільки цьому протидіє
натрій-калієвий насос.
Оскільки Na+ сам не може вийти з клітини, а К+ – надійти в
клітину проти своїх електрохімічних градієнтів, вони повинні активно переміщуватися
крізь мембрану.
У формуванні МПС
натрій-калієвий насос виконує дві функції: 1) підтримує трансмембранний
градієнт концентрацій Na+ і К+; 2) генерує певну
різницю потенціалів, яка додається до потенціалу, що створюється дифузією К+
за концентраційним градієнтом.
2.
Потенціал дії
Потенціалом дії (ПД) називають
швидке коливання МПС, що виникає під час збудження клітини. В основі ПД лежать
зміни електричної (іонної) провідності клітинної мембрани. Амплітуда і
тривалість ПД окремої клітини мало залежать від сили подразнення, важливо лише,
щоб ця сила досягла певного критичного значення – порогової сили
подразнення. ПД, що виникає у місці подразнення, поширюється вздовж
нервового чи м'язового волокна, не змінюючи своєї амплітуди. Наявність порогу
подразнення і незалежність амплітуди ПД від сили подразнення підпорядковується
закону "все або нічого".
У типовому
внутрішньоклітинному ПД розрізняють: 1) висхідну фазу; 2) пік (верхівку); 3)
низхідну фазу; 4) слідові потенціали. Встановлено, що під час висхідної
фази ПД відбувається не просто зникнення трансмембранної різниці потенціалів (деполяризація
мембрани), а виникає різниця потенціалів протилежного знака (овершут): внутрішня частина мембрани в ділянці
генерації ПД стає на певний час зарядженою позитивно відносно зовнішньої
частини мембрани, зарядженої негативно.
Під час низхідної
фази ПД відновлюється початкове значення МП (реполяризація
мембрани). Тривалість піку ПД різних збудливих тканин варіює від 0,5 до 3
мс. Зміни поляризації мембрани, які спостерігаються після завершення
високовольтної частини ПД (піку), називають слідовими
потенціалами. Розрізняють два види слідових
потенціалів – слідову деполяризацію (слідовий негативний потенціал) і слідову
гіперполяризацію (слідовий
позитивний потенціал), амплітуда яких не перевищує кількох мілівольт (5-10 %
рівня піку), а тривалість буває різною – від кількох мілісекунд
до десятків секунд.
Іонний механізм генерації ПД. В основі генерації
ПД лежать зміни проникності клітинної мембрани, що виникають послідовно за часом.
У момент подразнення провідність мембрани для Na+ зростає і Na+ починає надходити
в клітину, знижуючи внутрішній негативний заряд мембрани, тобто виникає
деполяризація клітинної мембрани. При досягненні мембраною певного – критичного
– рівня деполяризації виникає лавиноподібний потік Na+ всередину клітини,
що зумовлює появу висхідного коліна ПД.
Натрієва
провідність досягає максимуму менш ніж за 1 мс після початку ПД, а потім різко
знижується, зникаючи зовсім протягом 0,5 мс, хоча деполяризація мембрани ще
зберігається. Це явище називають натрієвою інактивацією, яка існує доти,
доки триває деполяризація мембрани. Натрієва активаційна система відновлюється,
коли МПС повертається до початкового рівня або навіть при певній гіперполяризації мембрани.
Зміни збудливості клітини під час збудження. Під час натрієвої
інактивації будь-яка деполяризація мембрани абсолютно неефективна, тобто
клітина в цей час незбудлива. Це абсолютний рефрактерний період, який
триває 1-2 мс. Потім протягом кількох мілісекунд після
закінчення абсолютної рефрактерності нове збудження можна викликати лише
більшою силою подразнення, ніж перший ПД. Значення ПД в цей час також зменшене,
оскільки натрієва система не повністю відновлена після інактивації під час
першого ПД. Цей відрізок часу, протягом якого відбувається відновлення
збудливості клітини, називають відносним рефрактерним періодом.
У живій клітині
існують дві системи руху іонів крізь мембрану. Одна з них здійснюється за
градієнтом концентрації іонів і не потребує витрати енергії – це пасивний
іонний транспорт. Він відповідає за підтримання МПС і виникнення ПД,
здійснюється через іонні канали. Друга система руху іонів крізь мембрану
відбувається проти концентраційного градієнта і полягає у
"викачуванні" Na+ з цитоплазми і "закачуванні" К+
всередину клітини за допомогою іонних насосів. Цей механізм можливий
тільки з витратами енергії і називається активним іонним транспортом.
Функції іонних каналів. У клітинній
мембрані існують пори, або канали. Терміном "канал" позначають
той шлях, яким іони проходять крізь мембрану за електрохімічним градієнтом. У
клітинній мембрані існує кілька різних іонних каналів: селективних та неселективних.
Перші пропускають лише якийсь певний іон: Na+, K+ або Са2+,
а другі – кілька іонів.
Кальцієві канали. Ретельне
дослідження функції іонних каналів різних нервових клітин дало змогу
модифікувати іонну модель генерації ПД, запропоновану Ходжкіним
і Хакслі, до якої входили лише натрієві й калієві
канали. Виявилося, що Са2+ також беруть активну участь у генерації
ПД.
Селективність
(вибірковість) кальцієвих каналів зумовлена наявністю в ділянці зовнішнього
входу хімічних груп, які мають підвищену спорідненість до двовалентних
катіонів: іони кальцію зв'язуються з такими групами і тільки після цього
проходять до порожнини каналу.
Характерною
особливістю кальцієвих каналів є залежність їх від клітинного метаболізму. Йони
кальцію ефективно впливають на синтез білків і забезпечують транспорт утворених
молекул до аксонів і дендритів. Відкриття цього явища безпосередньо свідчило
про те, що процеси на мембрані прямо пов'язані з процесами всередині клітини.
3.
Механізм
проведення збудження нервовими волокнами
Проведення
збудження вздовж нервових волокон здійснюється за допомогою місцевих (локальних)
струмів, які виникають між збудженою (деполяризованою)
і нормально поляризованою ділянками волокна. Поширення локальних струмів уздовж
волокна визначається його кабельними властивостями, а напрямок струму такий, що
він викликає кателектротонічну деполяризацію
сусідньої зі збудженою ділянки мембрани. Деполяризація швидко досягає
порогового значення і генерує ПД, який, у свою чергу, активує наступну ділянку
волокна. Завдяки такому естафетному механізму збудження поширюється вздовж
усього волокна, причому в немієлінізованих і м'язових
волокнах збудження безперервно переходить від однієї точки клітинної мембрани
до іншої.
У немієлінізованих волокнах швидкість поширення ПД залежить і
від опору аксоплазми аксона. Цей опір, у свою чергу, зумовлений діаметром
волокна: чим менший діаметр, тим більший опір. У тонких аксонах великий опір
аксоплазми негативно впливає на електричну провідність і зменшує довжину
локального ланцюга, до якого входить тільки та ділянка, що розміщена
безпосередньо попереду від ПД. Тому швидкість поширення збудження в тонких
волокнах найменша (до 0,5 м/с).
У хребетних
збільшення швидкості проведення збудження відбувається за рахунок покриття
волокон мієліновою оболонкою. Мієлінова оболонка нервового волокна має високий
питомий опір (500-800 Ом ´ см2) і
виконує роль ізолятора, який переривається через кожні 1-2 мм вузлами нервового
волокна (перетяжками Ранв'є). Це запобігає втраті
струму між ними. Завдяки цим властивостям локальні струми від збудженого вузла
не входять у ділянки між вузлами, а деполяризують
наступний вузол. При цьому ПД виникають тільки у вузлах нервового волокна.
Такий механізм поширення збудження називають стрибкоподібним (сальтаторним). Він економічніший,
надійніший (збудження може перестрибнути через 1-2 вузли), швидший, тобто
загалом має вищий чинник надійності.
Розмір ділянки
волокна, в якій розвивається збудження, залежить також від амплітуди ПД: чим
більша його амплітуда, тим більша ділянка волокна охоплюється критичною
(пороговою) деполяризацією клітинної мембрани.
Закони проведення
збудження.
1.
Закон анатомічної і фізіологічної цілісності волокна – проведення
збудження в нерві можливе лише за умови його абсолютної цілості і нормального
функціонального стану. Проведення збудження порушується після перерізання нервових волокон, у разі блокади натрієвих
каналів у випадках різкого локального охолодження тощо.
2.
Закон двобічного проведення збудження. У природних
умовах в організмі збудження в кожному нервовому волокні поширюється тільки в
одному напрямку, а зворотний шлях йому перекрито рефрактерністю
раніше збудженої ділянки.
3.
Закон ізольованого проведення збудження. У нервовому стовбурі всі волокна омиваються міжклітинною
рідиною, яка є добрим провідником електричного струму. Якщо одне з цих волокон
працює, то зовнішні петлі струму, тобто локальні струми, що виникають під час
поширення ПД, потрапляють до сусідніх волокон, які становлять частину
зовнішнього провідного середовища. Проте сила цих локальних струмів за
активності невеликої кількості волокон дуже мала і її не вистачає для
подразнення сусідніх волокон.
4.
Посмуговані м'язи
Класифікація. Традиційно
виділяють три види м'язів: посмуговані, гладкі і посмугований серцевий.
Поперечна смугастість зумовлена чергуванням ділянок з різним заломленням
світла, що помітно під світловим мікроскопом.
Посмуговані м'язи
складаються з волокон (симпластів) двох типів. Червоні м'язи мають
тонкі волокна, багаті на саркоплазму, де міститься значна кількість ядер і мало
м'язових міофібрил, до того ж розміщених групами по
3-10. У саркоплазмі цих м'язів міститься пігмент міоглобін, який,
подібно до гемоглобіну крові, здатний зв'язувати й віддавати кисень. М'язи, що
містять товсті волокна і значно більше міофібрил,
рівномірно розподілених у саркоплазмі, мають світліший колір і тому називаються
білими.
Ті м'язи, які
щодня і майже безперервно працюють, забезпечуючи певну позу називають статичними,
або тонічними, м'язами. Вони мають будову, властиву червоним м'язам.
М'язи, які здійснюють швидкі й сильні скорочення, є білими. їх ще називають фазними,
або тетанічними, м'язами.
У людини
співвідношення червоних і білих м'язових волокон різне в різних м'язах. Це
залежить від функції, яку виконує м'яз. Червоні волокна беруть участь у рухах,
де потрібна витривалість і ритмічність: ходіння, біг, плавання, підтримання
вертикального положення тіла. Білі волокна забезпечують здійснення важкої, але
нетривалої роботи. У дітей спочатку взагалі немає розподілу на білі й червоні
м'язи, їхні м'язові волокна однорідні і за своїми властивостями ближчі до
червоних. Ось чому діти можуть гратися годинами, не стомлюючись.
Проте у підлітків
10-13 років відбувається певний спад м'язової активності. Це пов'язано з ростом
тіла: верхні й нижні кінцівки подовжуються, кровоносні судини також
видовжуються, але аорта залишається поки що вузькою, і серце відстає порівняно
з ростом тіла. При цьому м'язи зазнають справжнього кисневого голодування і
швидко стомлюються. Через кілька років серце й аорта досягають нормальних
розмірів і все набуває відповідності. Саме тоді завершується поділ м'язів на
білі та червоні, яких у дорослої людини приблизно порівну, хоча у кожної це
співвідношення залежить від спадковості, тренованості, способу життя тощо.
Нервово-рухова одиниця. Руховий нейрон
разом із м'язовими волокнами, які він іннервує, називають нервово-руховою (нейромоторною), або руховою (моторною), одиницею (РО).
Всередині м'яза
рухове нервове волокно, що відходить від тіла рухового нейрона, розгалужується
й іннервує цілу групу м'язових клітин. Тому стимуляція одного рухового нейрона
чи його аксона зумовлює одночасне збудження всієї групи м'язових клітин.
За будовою
розрізняють малі й великі РО, а за функцією – тонічні (повільні)
й фазні (швидкі). Малі РО іннервуються
тонким аксоном з кількома кінцевими гілочками, які охоплюють тільки 10-12
волокон м'яза, утворюючи на кожному з них лише одне нервово-м'язове сполучення.
Вони входять до складу м'язів лиця, кистей, пальців рук і рідше – великих
м'язів тулуба й кінцівок. Великі РО іннервуються
відносно товстими аксонами, які утворюють велику кількість розгалужень, що
закінчуються на тисячах м'язових волокон, утворюючи на них численні
нервово-м'язові сполучення. Великі РО входять переважно до складу великих
м'язів тулуба й кінцівок, вони мають вищий поріг збудливості, стійку імпульсну
активність, високу витривалість і розвивають значну силу. Великі РО здатні без
зниження частоти імпульсів працювати десятки хвилин, тому їх називають нестомлюваними. Практично кожен м'яз містить
як великі, так і малі РО.
М'язові волокна у
тонічних і фазних РО мають різну будову. Фазні– товщі, мають
більшу кількість міофібрил і тому розвивають більшу
силу, ніж тонічні. Тонічні волокна мають добре розвинену
капілярну сітку, що забезпечує краще кровопостачання їх, підвищену кількість
міоглобіну в крові, який підтримує деякий час кисневий гомеостаз і після
припинення надходження кисню. Тонічні РО входять до складу червоних м'язів, а
фазні переважають у білих м'язах. Фазні РО вмикаються на початку скорочення, що
забезпечує швидке зростання м'язового напруження. Фазні й тонічні РО
функціонують одночасно, коли потрібно розвинути велике напруження у разі
статичних і динамічних м'язових зусиль.
Фазні м'язові
волокна гірше постачаються киснем крові, а тому мають високу активність гліколітичних процесів і підвищений вміст глікогену. Вони
не здатні до тривалої роботи, але пристосовані до сильніших і швидких, хоча
короткочасних, м'язових скорочень.
Будова м'язів
залежить від функції, яку вони виконують. У ссавців усі м'язи мають як тонічні,
так і фазні волокна, але кількість їх визначається функцією. У людей з віком
кількість фазних м'язових волокон зменшується.
Усі м'язові
волокна мають три найважливіші властивості: збудливість, провідність і скоротливість.
У природних умовах збудження і скорочення м'язів викликаються нервовими
імпульсами, що надходять до м'язових волокон від рухових нейронів головного і
спинного мозку.
Типи м'язових
скорочень. Характер скорочення посмугованого м'яза залежить від
частоти подразнення або імпуль-сації рухових
нейронів, що його іннер-вують.
Поодиноке
скорочення. У відповідь на один нервовий імпульс відбувається швидке
скорочення, за яким настає швидке розслаблення м'яза. Цей процес називають поодиноким
скороченням.
Амплітуда
поодинокого скорочення ізольованого м'язового волокна не залежить від сили
подразнення, тобто підпорядковується закону "все або нічого". Проте
скорочення цілого м'яза, що складається з багатьох м'язових волокон з різною
збудливістю, безпосередньо залежить від сили подразнення: за порогової сили
подразнення до реакції залучається лише невелика частина волокон і скорочення
м'яза має малу (порогову) амплітуду, зі збільшенням сили подразнення кількість
волокон, охоплених збудженням, зростає, скорочення посилюється доти, доки всі
волокна не скоротяться. Це максимальне скорочення, і подальше підвищення
сили подразнення вже не збільшує його амплітуду.
Якщо в умовах
експерименту зафіксувати м'яз з обох кінців, то під час подразнення він буде
розвивати лише напруження, не змінюючи своєї довжини. Цей тип скорочення
називають ізометричним. Якщо один кінець м'яза не фіксувати, то під час
подразнення м'яз скорочуватиметься, не змінюючи свого напруження. Таке
скорочення називають ізотонічним. Якщо м'яз під час скорочення долає
якийсь опір, то скорочення називають концентричним. У разі значного
навантаження м'яз розтягується, незважаючи на своє максимальне напруження, – це
ексцентричний тип скорочення.
Розрізняють також
два режими скорочення: динамічний, коли м'яз почергово скорочується і
розслаблюється, і статичний, коли м'яз, тривало напружуючись, не може
подолати опір. Цей режим властивий ізометричному скороченню.
Тетанічне
скорочення. Якщо на окреме м'язове волокно чи на весь м'яз діють два
субмаксимальні подразнення з невеликим інтервалом між ними, то скорочення, що
виникає, матиме більшу амплітуду, ніж максимальне при поодинокому подразненні,
оскільки скоротливі ефекти, спричинені першим і другим подразненнями, ніби
додаються. Це явище називають сумацією скорочень.
Для виникнення
такого скорочення потрібно, щоб інтервал часу між подразненнями перевищував
тривалість рефрактерного періоду, інакше на друге подразнення не буде
відповіді, але був коротшим за тривалість усього скорочення, щоб друге
подразнення подіяло на м'яз раніше, ніж він встигне розслабитися після першого
подразнення.
За ритмічного
подразнення м'яза, коли хвилі скорочення накладаються одна на одну (суперпозиція),
розвивається тривале скорочення м'яза, яке називають тетанічним, або
тетанусом. Таке скорочення відбувається лише тоді, коли кожний наступний
імпульс надходить ще до закінчення хвилі попереднього скорочення.
Тонічне
скорочення. Тонічним називають тривале скорочення м'яза, яке
відбувається з незначними енергетичними витратами і дуже повільним розвитком втомлення. Тонічні скорочення найбільш характерні для
гладких м'язів, але серед посмугованих м'язів також є чимало тонічних. До таких
належать насамперед скелетні м'язи, що підтримують вертикальне положення тіла
людини (антигравітаційні м'язи): м'язи спини,
шиї, м'язи, що підтримують нижню щелепу. Ці м'язи годинами перебувають у
скороченому стані, витримуючи вагу щелеп, голови чи верхньої половини тулуба, і
при цьому, як правило, втомлення у цих м'язах не
розвивається. Аналіз електроміограми свідчить, що в підтриманні тонусу м'язів
важливу роль відіграють чергування скорочень і розслаблень тонічних (повільних)
РО в асинхронному режимі.
5.
Механізм м'язового
скорочення
Будова і функція
будь-якої системи тісно взаємопов'язані, і на підставі вивчення макро- чи
мікроструктури системи можна скласти уявлення про механізми її функціонування.
Будова м'язового
волокна. Структурно-функціональною одиницею м'яза є м'язове
волокно. У посмугованих м'язах – це багатоядерна (близько 100 ядер) клітина
(міосимпласт), що утворилася злиттям первинних
м'язових клітин – міобластів. М'язове волокно має циліндричну форму,
товщина його коливається від 10 до 100 мкм, а довжина від кількох міліметрів до
кількох (іноді десятків) сантиметрів. Зовні волокно вкрите оболонкою (сарколемою), яка виконує функцію еластичного футляра і
забезпечує його пружність. Під сарколемою
міститься саркоплазма.
Саркоплазма – це рідина, в
якій містяться скоротливі елементи м'язового волокна – міофібрили.
У цій рідині містяться також розчинені білки,: зокрема міоглобін,
гранули глікогену, краплини жиру тощо.
Міофібрила складається з двох
типів тонких ниток – міофіламентів (протофібрил):
товстих (діаметром 10-15 нм, завдовжки 1,6 мкм), утворених скоротливим
білком міозином і тонких (діаметром 5-7 нм, завдовжки 1 мкм),
утворених білком актином.
Хімічні перетворення та енергетика м'яза
Хімічні реакції як
джерело енергії м'яза. Безпосереднім джерелом енергії для скорочення м'яза є
АТФ. У зв'язку з тим, що резерв АТФ у клітині обмежений, він має постійно
відновлюватися за рахунок інших джерел енергії. Ресинтез
АТФ може відбуватися двома шляхами: анаеробно
та аеробно.
Анаеробний ресинтез АТФ здійснюється насамперед за рахунок
перенесення фосфатної групи від багатого на енергію креатиифосфату
на АДФ (фосфогенна система), а також завдяки
розщепленню глюкози (гліколітична система). Внаслідок
реакції гліколізу (анаеробного окиснення) з однієї молекули глюкози
утворюється по 2 молекули АТФ і молочної кислоти (лактату), а з глікогену – 3
молекули АТФ і 2 – лактату.
Аеробний ресинтез АТФ відбувається за рахунок окиснення таких
багатих на енергію сполук, як вуглеводи й ліпіди. Потужність анаеробної системи
у 9 разів перевищує потужність аеробної (окиснення ліпідів), проте ємність
останньої у 12 000 разів більша за анаеробну. Тому є підстави вважати, що
анаеробні системи забезпечують виконання швидких рухів, а за рахунок окиснення
ліпідів може тривалий час здійснюватися менш інтенсивна робота.
Теплопродукція
м'яза. Під час скорочення м'яза відбувається посилене
розщеплення АТФ, інтенсивність обміну речовин зростає у тисячу разів.
Відповідно збільшується утворення і виділення теплової енергії м'язом. А. Хіл за допомогою сконструйованих ним чутливих термопар
установив, що 1 г скелетного м'яза жаби виділяє 0,00002 Дж
(0,006 кал) теплової енергії за одне скорочення, і розділив теплотворення м'яза
на дві фази.
Фаза початкового
теплотворення починається з моменту збудження м'яза і триває протягом
усього скорочення. Цю фазу поділяють на теплотворення активації,
теплотворення вкорочення і теплотворення розслаблення. Теплова
енергія активації виділяється м'язом з початку порогового чи сильнішого подразнення
і впродовж періоду збудження. Вона виробляється і в умовах ізометричного
напруження. А коли м'яз здійснює механічну роботу (наприклад, під час
піднімання вантажу), відбувається розщеплення додаткової кількості АТФ і
виділяється додаткова теплова енергія скорочення, пропорційна виконаній роботі.
Розслаблення м'яза також потребує витрат енергії, про що свідчить виділення
теплової енергії під час цього процесу. Фаза початкового теплотворення
відбувається в анаеробних умовах і зумовлена виділенням енергії внаслідок
розщеплення АТФ і гліколізу.
Фаза затриманого,
або відновного, теплотворення, на відміну від попередньої фази,
потребує обов'язкової наявності кисню. Ця фаза пов'язана з ви-
діленням енергії
окиснення молочної і піровиноградної кислот, які
утворюються під час скорочення. Відбувається фосфорилу-вання
АДФ і креатину до відновлення АТФ і креатинфосфату.
Кількісно теплотворення цієї фази приблизно дорівнює теплотворенню першої фази,
але триває майже у 1000 разів довше.
Робота і стомлення м'язів
Під час скорочення
м'яз виконує певну роботу, значення її залежить від сили м'яза.
Сила м'яза. Окреме м'язове
волокно здатне розвинути силу (0,98-2,9) · 10-3 Н. Товсті міофібрили розвивають більшу силу, ніж тонкі. Сила м'яза
залежить також від кількості одночасно працюючих його м'язових волокон (від 3
до 80 %), а також від довжини, яку має м'яз на початку скорочення (попередньо
розтягнутий м'яз скорочується сильніше). Регуляція ступеня напруження м'яза
здійснюється двома шляхами: залученням більшої кількості м'язових волокон у
процес скорочення і зміною частоти скорочень м'яза.
Максимальною
вважають силу, яку розвиває м'яз під час скорочення, коли він ледве зрушує з
місця максимальний вантаж. Для визначення абсолютної сили м'яза його
максимальну силу треба поділити на площу фізіологічного перерізу м'яза,
перпендикулярну до його волокон (мал. 132). У табл. 20 наведено значення
абсолютної сили м'язів у різних тварин.
Людина у
повсякденному житті розвиває максимальну силу своїх м'язів тільки тоді, коли
м'язи при цьому не вкорочуються або вкорочуються дуже незначно, наприклад, коли
людина на щось натискає або тягне занадто важкий тягар. Навпаки, людина здатна
робити дуже швидкі рухи тільки за невеликого м'язового навантаження, наприклад
під час гри на гітарі чи роялі.
Робота м'яза. Під час будь-якого
скорочення м'яз виконує внутрішню роботу, пов'язану з процесами, які
відбуваються у м'язовому волокні: рух йонів під час збудження, скорочення і
після нього, тертя, втрати енергії у процесі ресинтезу
АТФ тощо. Кількісно цю роботу визначають за інтенсивністю споживання кисню.
Зовнішня (механічна) робота
виконується лише під час переміщення будь-якого вантажу, тіла або його
частин у просторі. Механічна робота м'яза (А) вимірюється
добутком ваги піднятого вантажу (Р) на вкорочення м'яза (l), тобто А = Р ·
l. Проте м'яз має
таку цікаву властивість – при поступовому збільшенні вантажу його вкорочення
при тому самому подразненні спочатку зростає, а потім поступово зменшується і
за певних значень важкого вантажу дорівнює нулю. Звідси випливає, що у кожного
м'яза максимальна робота можлива лише при певних середніх навантаженнях. Це є закон
середніх навантажень, який випливає із залежності сили скорочення м'яза від
його довжини.
Відношення
зовнішньої роботи м'яза до його внутрішньої роботи називається коефіцієнтом
корисної дії (ККД). Його значення залежить від навантаження і коливається в
межах 30-50 %, що можна порівняти з ККД дизельного двигуна (37-41 %). Треновані
м'язи працюють набагато економніше, ніж нетреновані, крім того, внаслідок
тренування м язи стають сильнішими і витривалішими.
Під час тривалої
м'язової роботи відбувається головним чином аеробний ресинтез
АТФ за рахунок оксидного фосфорилування. Необхідна
для цього енергія надходить завдяки окисненню вуглеводів і ліпідів. За умови,
що швидкість утворення АТФ дорівнює швидкості його розщеплення, система
перебуває у рівноважному стані, вміст АТФ і креатинфосфату
не змінюється.
Під час виконання
спортивних вправ, які потребують витривалості, швидкість розщеплення АТФ значно
зростає порівняно зі станом спокою. При цьому мусить збільшуватися швидкість ресинтезу АТФ, що можливо при швидкому надходженні у м'яз
кисню і глюкози. Внаслідок місцевого розширення кровоносних судин швидкість
кровотоку в м'язі зростає до 20 разів (робоча гіперемія), хвилинний
об'єм крові, частота скорочень серця і дихання збільшуються у 2-3 рази.
Перед закінченням
тривалої виснажливої роботи можливий так званий фінішний ривок, зумовлений
розщепленням додаткової кількості глікогену анаеробним шляхом за допомогою
гліколізу. Під час цієї реакції утворення АТФ відбувається у 2-3 рази швидше,
що відповідно забезпечує зростання у 2-3 рази механічної роботи. Щоправда,
через обмеженість резервів анаеробної енергії граничний час для такої посиленої
роботи не перевищує 30 с.
Стомлення м'яза. Стомленням
називають тимчасове зниження працездатності клітини, органа чи цілого
організму, яке настає внаслідок їхньої роботи і зникає після відпочинку.
Стомлення
ізольованих скелетних м'язів, яке виявляється поступовим зменшенням і
припиненням скорочень, виникає внаслідок накопичення у м'язах (всередині
волокон і в міжклітинному просторі) певних продуктів обміну речовин, переважно
молочної (лактату), а також фосфатної кислот. Ці речовини порушують функцію
м'язових і нервових структур, насамперед нервово-м'язову передачу. У свою
чергу, накопичення лактату зумовлюється нестачею кисню. Що стосується
енергетичних ресурсів м'яза (глікогену для синтезу АТФ і креатинфосфату),
то вони в таких умовах під час розвитку стомлення не вичерпуються.
В природних умовах
стомлення розвивається передусім внаслідок стомлення структур ЦНС, оскільки
пряма стимуляція стомленого м'яза викликає нормальний скоротливий ефект.
Досить переконливим
доказом значення нервових центрів у розвитку стомлення можуть бути досліди з
навіюванням. Так, перебуваючи у гіпнотичному стані, піддослідний може тривалий
час піднімати важку гирю, якщо йому навіяти, що у нього в руці легкий кошик. І
навпаки, при навіюванні піддослідному, що йому дали важку гирю, стомлення
швидко розвивається при підніманні легкого кошика. При цьому зміни частоти
скорочень серця і дихання та газообміну відповідають не реальній роботі, яку
здійснює піддослідний, а тій, яка йому навіяна.
Під час напруженої
м'язової роботи, через 3-5 хв після її початку, часто настають особливі стани –
"мертвої точки" і "другого дихання". "Мертва
точка" – це стан тимчасового зниження працездатності людини, а "друге
дихання" – це стан, що настає після її подолання, з суб'єктивним
відчуттям полегшення під час виконання роботи.
У сталі
"мертвої точки" стрімко зростає споживання кисню і виділення
вуглекислого газу, прискорюється, стає більш поверхневим і уривчастим дихання,
порушується координація рухів, знижується інтенсивність роботи, підвищуються
витрати енергії, знижується ККД.
Під час
"другого дихання" різко підвищується потовиділення, поліпшуються
кровопостачання м'язів і периферична циркуляція крові, у м'язах зростає
швидкість біохімічних процесів, яка забезпечує їх кращу працездатність.
"Мертва
точка" настає внаслідок тимчасового порушення на рівні ЦНС узгодженості у
функції рухового апарату і внутрішніх органів. Стан "мертвої точки"
переборюється завдяки значному вольовому зусиллю. При виході з "мертвої
точки" знижується гальмівний процес у мозку, відновлюється нормальний
баланс нервових процесів, зміцнюється рухова домінанта, відновлюється
коригувальна здатність кори головного мозку.
Відомо, що фізичні
вправи сприяють фізіологічній гіпертрофії м'язів, яка може бути саркоплазматичною або фібрилярною.
Саркоплазматичний тип гіпертрофії м'язів
– у м'язах збільшується об'єм саркоплазматичного матриксу і поживних речовин, зростають резерви глікогену,
збільшується кількість капілярів. Проте це мало впливає на силу м'язів, хоча й
підвищує їхню витривалість.
Міофібрилярному типу гіпертрофії м'язів властиве
збільшення об'єму міофібрил.
6.
Особливості гладких м'язів
Будова гладких
м'язів. Гладкі м'язи хребетних, які створюють м'язові шари
шлунка, кишок, сечоводів, бронхів, кровоносних судин та інших внутрішніх
органів, побудовані з веретеноподібних одноядер-них
м'язових клітин 2–10 мкм завтовшки і 50-400 мкм завдовжки.
Окремі клітини у
гладких м'язах зв'язані між собою низькоомними
електричними контактами – нексусами. Гладком'язові клітини мають невелику кількість міофібрил, що переважно містять тонкі (актинові) міофіламенти. Виявлено також і міозинові міофіламенти, проте упорядкованості їх розміщення, як у
посмугованих м'язах, немає, тому посмугованості
гладкі м'язи позбавлені. Однак наявність обох видів міофіламентів
свідчить про один і той самий скоротливий механізм як у посмугованих, так і в
гладких м'язах.
Електрична
активність гладких м'язів. Мембранний потенціал спокою гладких м'язових клітин
становить 60-70 мВ. Деякі клітини виявляють здатність до періодичної спонтанної
деполяризації. При цьому на їхній клітинній мембрані розвиваються повільні
хвилі, і коли така хвиля деполяризує мембрану до
критичного рівня (30-40 мВ), на її верхівці виникає один або кілька ПД амплітудою
кілька мілівольт. Це водії ритму (пейсмекери),
які завдяки своїй спонтанній активності забезпечують автоматизм шлунка, кишок
та інших внутрішніх органів.
На відміну від
посмугованих м'язів і нейронів ПД у гладких міоцитах
має кальцієву природу: він зумовлений відкриттям потенціалозалежних
кальцієвих каналів і надходженням Са2+ усередину клітини. Щ канали
за деякими властивостями відрізняються від натрієвих каналів: вони значно
повільніше активуються та інактивуються, і тому
кальцієві ПД тривають набагато довше, ніж натрієві. Вони поширюються в гладкій
м'язовій тканині зі швидкістю 0,05-0,1 м/с, створюючи її міогенний
тонус.
Скоротлива
активність гладких м'язів. Кожний ПД викликає поодиноке скорочення гладкої м'язової
клітини.
Сила скорочення
гладких м'язів хребетних практично така сама, як і скелетних м'язів (30-40 Н/см2),
проте витрата енергії гладкими м'язами (за однакового напруження) у 100-500
разів менша, що, ймовірно, пов'язано з особливою організацією скоротливого акту
гладких м'язів.
Тривалість
скорочення. Поодиноке скорочення гладкої м'язової клітини триває
кілька секунд. Висхідна фаза скорочення триває 1-2 с, а розслаблення – 5-10 с
(у м'язах кишок), тобто порівняно з посмугованим м'язом скорочення гладкого
м'яза відбувається у 20-50 разів повільніше. Це зумовлено низькою швидкістю
взаємодії скоротливих білків у гладких м'язових клітинах через низьку
активність їхньої АТФ-ази. У зв'язку з цим тетанічне скорочення гладких м'язів
виникає при частоті стимуляції 0,5-3 за 1 с.
Тонус гладких м'язів.
Гладкі м'язи, що входять до складу стінки внутрішніх
порожнистих органів (шлунка, кишок тощо), можуть перебувати у скороченому стані
годинами, а гладкий м'яз матки ссавців взагалі скорочений майже все життя без
будь-яких ознак втоми, за винятком відносно коротких періодів вагітності.
Спонтанна
активність гладких м'язів. Періодичні зміни частоти генерації ПД клітинами – водіями
ритму (під впливом нервової системи або гуморальних чинників) створюють
коливання м'язового тонусу і складніші форми рухової функції гладких м'язів.
Проте багато які з гладких м'язів (зокрема, травного каналу, лімфатичних судин,
сечового міхура) є спонтанно активними. Ця спонтанна активність має міогенну природу, в основі якої лежить висока чутливість
клітинної мембрани гладких міоцитів до розтягання. Періодичне розтягання
спричинює деполяризацію клітинної мембрани і виникнення ПД, які вмикають
скоротливий апарат клітини. Чим сильніше розтягання, тим більша деполяризація
мембрани, вища частота генерації ПД і більше скорочення м'язів.
Ця підвищена
збудливість гладких м'язових структур є дуже важливою для функціонування
порожнистих органів, таких як кишки, кровоносні судини, сечовий міхур, матка,
сечоводи. Наповнення цих органів генерує підвищену активність гладких м'язів,
які їх утворюють. Навіть при порушенні нервової регуляції внутрішніх органів їх
функція може здійснюватися автоматично (хоча й не так досконало:
наприклад, сечовий міхур спорожнюється після наповнення, але не до кінця). Це
явище лежить в основі периферичної саморегуляції тонусу гладких м'язів
внутрішніх органів. Така саморегуляція можлива ще тому, що електрична
активність легко поширюється від клітини до клітини через низькоомні
нексуси. Внаслідок цього електрична активність
багатьох клітин синхронізується.
Іннервація і
регуляція тонусу гладких м'язів. Гладкі м'язи іннервуються
волокнами симпатичної і парасимпатичної частин автономної нервової системи.
Проте не всі м'язові клітини іннервуються, багато які
з них контролюються нервовою системою не прямо, а через нексуси.
Гладкі м'язи різних органів реагують на імпульси однієї й тієї самої іннервації
протилежним чином: наприклад, симпатичні нервові волокна звужують кровоносні
судини і розслаблюють шлунок і кишки. Така сама картина спостерігається
стосовно дії медіаторів та інших фізіологічно активних речовин. Так, адреналін
і норадреналін, медіатори симпатичної нервової системи, здійснюють
гальмівний вплив на несфінктерні гладкі м'язи
травного каналу, сечового міхура і бронхів, виявляючи збуджувальний вплив на
гладкі м'язи кровоносних судин. Ацетилхолін, медіатор парасимпатичної
нервової системи, збуджує гладкі м'язи травного каналу, бронхів і секреторних
органів і впливає гальмівним чином на м'язи кровоносних судин. Протилежний
вплив фізіологічно активних речовин на гладкі м'язи різних органів пов'язують з
властивостями Са2+-каналів та їх станом. Якщо вони у гладких м'язах,
наприклад шлунка, відкриті, то адреналін їх закриває, кальцій з м'язових
волокон викачується Са2+-насосом і волокно, а отже, і весь шлунок
розслаблюються. Навпаки, ацетилхолін відкриває ще більшу кількість Са2+-каналів,
концентрація Са2+ у саркоплазматичному
матриксі зростає, гладкі м'язи, а отже, шлунок скорочуються.
7.
Міжклітинна передача збудження і гальмування
У нервовій системі
кожний нейрон анатомічно відокремлений від інших нейронів та іннервованих тканин. Збудження і гальмування передаються з
однієї нервової клітини на іншу або з рухових нервових закінчень на клітини ефекторних органів через спеціальні структури міжклітинних
фізіологічних контактів – синапси. Саме ці контакти зумовлюють однобічне
проведення збудження в рефлекторній дузі та його сповільнення порівняно з часом
проведення збудження в нервових волокнах. Залежно від будови і функціонування
розрізняють хімічні та електричні шнапси.
Класифікація
синапсів. Міжклітинна передача імпульсів здійснюється за допомогою
трьох типів міжклітинних контактів: хімічних і електричних синапсів та
нексусів.
Хімічним (пухирцевим) синапсам властива широка синаптична щілина (20-50 нм), яка відокремлює пресинаптичні мембрану і ущільнення від постсинаптичних.
Збудження і гальмівні впливи передаються в цих синапсах в одному напрямку за
допомогою медіаторів. У електричних (безпухирцевих)
синапсах зовнішні шари мембрани контактуючих клітин розділені
простором завширшки 2 нм, вони функціонують за рахунок іонного струму.
Нексуси, або щільні
контакти, характеризуються майже повним злиттям зовнішніх шарів мембран
контактуючих клітин і значним стоншенням спільної ділянки мембрани обох клітин.
Нексусам властивий низький опір і висока двобічна проникність для іонів. Вони
здійснюють міжклітинну передачу збудження в серцевому м'язі та гладкій
мускулатурі.
Залежно від того,
між якими частинами нейронів утворений синапс, його називають аксодендритним, аксосоматичним
і аксоаксонним. У ядрах таламуса виявлено дендродендритні, дендросоматичні
та соматосоматичні синапси.
Хімічна передача збудження і гальмування
Після відкриття
електричних явищ у живих тканинах протягом майже 150 років у фізіології
домінували теорії електричної передачі збудження і гальмування як через нерви,
так і через синаптичні сполучення. І тільки у 1921 р.
австрійським фармаколом О. Леві було доведено, що
передача гальмівного впливу блукаючого нерва на серце здійснюється за допомогою
хімічної речовини – медіатору. Згодом медіаторна
теорія передачі сигналів у нервовій системі стала загальновизнаною.
Будова хімічних (пухирцевих) синапсів. Хімічні синапси
складаються з пресинаптичної частини, синаптичної щілини і субсинаптичної
мембрани. Пресинаптична частина – це
кінцеве розширення пресинаптичного нервового волокна.
Мембрану пресинаптичного ущільнення називають пресинаптичною, а частину мембрани постсинаптичної структури, розміщену під нею, – постсинаптичною. У посмугованих м'язових
волокнах ділянку мембрани під пресинаптичною частиною
називають кінцевою пластинкою. Субсинаптична
мембрана є хемозбудливою завдяки наявності в ній
численних рецепторів, які активуються медіаторами – речовинами, що
виділяються пресинаптичною частиною синапсу.
Типовим прикладом
хімічного синапсу є нервово-м'язовий контакт. Особливістю хімічних синапсів є
наявність у пресинаптичних нервових закінченнях пресинаптичних пухирців (діаметр у ЦНС 20-30
нм; а в нервово-м'язовому сипапсі – 50
нм). їх кількість в одному закінченні досягає 200-300 тис, і в кожному з них
міститься від 1 до 20 тис. молекул ацетилхоліну, який є медіатором у
нервово-м'язових синапсах скелетних м'язів. Вивільнення медіатору в синаптичну щілину відбувається шляхом екзоцитозу
– злиттям мембран пухирця і пресинаптичного
закінчення з наступним розривом їх і виходом медіатору в синаптичну
щілину. У синапсі в стані спокою відбувається
спонтанний розрив поодиноких пухирців і вивільнення з них кванта медіатору –
майже всіх молекул ацетилхоліну, що містились у одному пухирці. Під час збудження
у відповідь на один ПД вивільняється 100-300 квантів ацетилхоліну. У пухирцях в
ЦНС і периферичних вузлах містяться також інші медіатори: норадреналін,
амінокислоти, пептиди тощо. За формою, розмірами, оптичною густиною пухирців
іноді вдається розрізняти їхній вміст.
Синаптична щілина на посмугованих
м'язах має ширину 20-50 нм, а на гладких – від 10 (сім'явиносна
протока) до 4000 нм (легенева артерія). Вона вільно сполучається з міжклітинним
простором, заповнена гелеподібною рідиною.
Постсинаптична мембрана є частиною
мембрани постсинаптичної клітини, як правило, без
будь-якої морфологічної спеціалізації. Щоправда, постсинаптична
мембрана фазних м'язових клітин утворює численні складки, завдяки чому її
поверхня значно збільшується, досягаючи 10000 мкм2 на один синапс. Постсинаптична мембрана містить іонні потенціалонезалежні,
але хемочутливі канали, які активуються медіатором.
Синаптична передача
збудження. Згідно з сучасними уявленнями, передача збудження через
хімічні синапси відбувається у такій послідовності: пресинап-тичний
ПД спричинює виділення нервовим закінченням збудливого медіатору, який дифундує
крізь синаптичну щілину до субсинаптичної
мембрани, де відбувається його взаємодія з хеморецепторами, внаслідок чого
виникає зміна йонної проникності субсинаптичної
мембрани (Рис. 1, в – Б). Йонні струми
викликають деполяризацію цієї мембрани у вигляді збуджувального постсинаптичного потенціалу (ЗПСП).
Рисунок 1.
Холінорецептор електричного органа риби
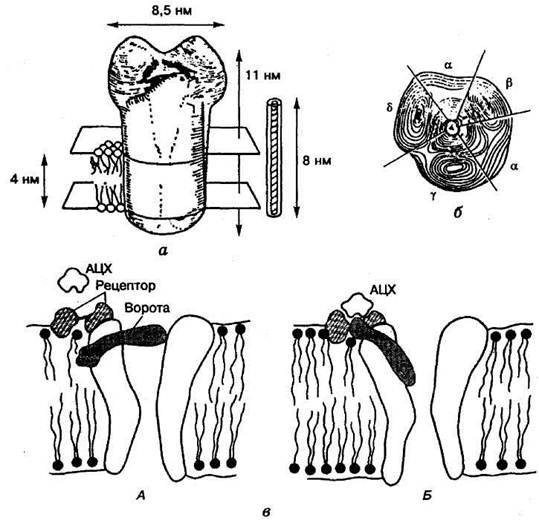
тривимірне зображення рецептора збоку (а) і згори
(б); в – активація рецептора ацетилхоліном (АЦХ)і А – ворота
зачинені; Б – ворота відчинені
Дифузія медіатору
крізь синаптичну щілину, на що витрачається певний
час, зумовлює синаптичну затримку.
Синаптична передача
гальмівних впливів. У хімічних синапсах відбувається також передача
гальмівних впливів. Гальмування розвивається на постсинаптичній
мембрані услід за збудженням пресинаптичної мембрани.
Саме тому деякі автори вважають, що краще говорити про передачу через синапси гальмівних
впливів, а не гальмування, якого позбавлена пресинаптична
структура.
Отже, гальмівні
синапси здійснюють трансформацію збудження на гальмування.
Механізм передачі
гальмівного впливу у хімічних синапсах полягає в тому, що внаслідок дії пресинаптичного ПД вивільняється гальмівний медіатор, який
дифундує до субсинаптичної мембрани. Це викликає
зміну йонної провідності мембрани і розвиток у ній гіперполяризації – гальмівного постсинаптичного потенціалу (ГПСП).
Песимальне гальмування. При дуже частому
подразненні нерва, що іннервує м'яз, ПКП підсумовуються на кожний імпульс,
оскільки в дуже короткий міжім-пульсний інтервал
холінестераза не встигає повністю розщепити виділюваний ацетилхолін. Унаслідок
сумації багатьох ПКП постсинаптична мембрана все
більше й більше деполяризується.
Ця деполяризація
лежить в основі песимального гальмування Введенського, суть якого полягає в тому, що за певної
оптимальної частоти стимуляції скорочення м'яза стає максимальним. Проте якщо
далі збільшувати цю частоту, то поступово сила скорочення зменшується і за
певної високої частоти подразнення м'яз майже повністю розслаблюється (песимум). Зменшення частоти стимуляції у цей момент
відразу ж викликає відновлення оптимального рівня м'язового скорочення (оптимум).
Песимальне гальмування виникає тому, що при збільшенні частоти
подразнення рефрактерна фаза після кожного наступного скорочення поступово
зростає і, коли її тривалість перевищить часовий інтервал між стимулами,
подразнення з оптимального перетворюється на песимальне.
Медіатори в
хімічних синапсах. Ще у 30-ті роки XX ст. було встановлено, що медіатором у
нервово-м'язовому синапсі є ацетилхолін.
Окрему групу
медіаторів становлять катехоламіни – адреналін,
норадреналін і дофамін, які
переважно є збуджувальними медіаторами у ЦНС. Ще одним гальмівним
медіатором, але вже постсинаптичного гальмування, є гліцин.
ЕЛЕКТРИЧНА
ПЕРЕДАЧА ЗБУДЖЕННЯ І ГАЛЬМУВАННЯ
У живому організмі
клітини постійно обмінюються між собою інформацією, причому головну роль у
цьому процесі відіграють хімічні речовини. Проте є чимало органів, клітини яких
здійснюють безпосередній (без участі нервової системи) обмін інформацією
електричним способом. Це насамперед відбувається у збудливих тканинах–
м'язових, а також секреторних. Між клітинами міокарда або гладких м'язів
існують сполучні плями (щільні контакти, нексуси),
через які збудження за допомогою йонних струмів
переходить з однієї клітини до іншої. Подібний механізм існує й між
секреторними клітинами. Ймовірно, що такі утвори є попередниками електричних
синапсів, які здійснюють передачу сигналів у ЦНС. Останні виявлено в нервовій
системі безхребетних і нижчих хребетних тварин, але у ссавців їх значно менше.
Електрична
передача збудження. Морфологічною умовою електричної передачі збудження є те,
що між мембранами контактуючих клітин щілина дуже вузька і має низький
електричний опір, що дає змогу ПД без перешкод поширюватися на постсинаптичну мембрану й у зворотному напрямку.
В електричних
синапсах відстань між пре- і постсинаптичиою
мембранами становить всього 2-4 нм і крізь синаптичну
щілину проходять містки з білкових часточок, своєрідні канали завширшки 1-1,5
нм, які пронизують пре- і постсинаптичну мембрани
синапсу. Через ці канали з клітини у клітину можуть переходити неорганічні йони і навіть невеликі молекули.
Електричні синапси
вмикаються насамперед тоді, коли потрібна дуже швидка передача збудження,
оскільки в них практично немає синаптичної затримки
або вона дуже мала. Ось чому електричні синапси знаходяться у структурах, що
здійснюють реакції втечі тварини, рятування від небезпеки тощо.
Отже, можна
зробити висновок, що хімічні й електричні синапси мають такі властивості:
1. У хімічних
синапсах є синаптична затримка (0,2-0,5 мс), що
уповільнює передачу сигналу. В електричних синапсах її немає або вона дуже
незначна.
2.Хімічні синапси
мають лише однобічну провідність, а більшість електричних синапсів проводять
збудження в обидвабоки – з пре- до постсинаптичної клітиниі навпаки.
3.Хімічні синапси
можуть бути збуджувальними або гальмівними (залежно відмедіатору),
а електричні переважно збуджувальними.
4.Хімічні синапси
значно краще, ніж електричні, зберігають сліди попередньої активності. Тому
хімічна передача може змінюватися під впливом різних чинників.
5.Хімічні синапси
значно чутливіші дозмін
температури їхнього середовища, ніжелектричні, що має
істотне значення для ЦНС теплокровних тварин.
6.Хімічні синапси є
досить надійними, оскільки мають високий ступінь гарантії(чинник синаптичної передачі 5 = 2).
БЛОКУВАННЯ
СИНАПТИЧНОЇ ПЕРЕДАЧІ
Цей процес добре
вивчений у нервово-м'язовому синапсі. Речовини, які
викликають розслаблення скелетних м'язів під час хірургічних операцій і в
деяких інших випадках, називають міорелаксантами.
Так, отрута кураре блокує нервово-м'язову передачу, конкуруючи з
ацетилхоліном за постсинаптичні рецептори. Ось чому
ця блокада залежить від концентрації обох речовин і може бути зворотною.

