Практичне
заняття №4.
Тема
"Розв’язування розрахункових задач з теми « Електрохімія "
Пригадайте матеріал і дайте відповіді на
запитання:
1. Що називається гальванічним елементом?
2. За яким принципом
записують схему гальванічного елемента?
3. Що називається стандартним електродним
потенціалом?
4. В
чому полягає сутність процесу електролізу? Що таке вихід за струмом?
5. Яка
принципова відмінність процесів, що відбуваються у гальванічному елементі та
при електролізі?
6.
Яке значення для електролізу має матеріал електрода?
7. Поясніть сутність процесів
гальваностегії та гальванопластики?
8. Чому
лужні метали не можна добути електролізом водних розчинів їхніх сполук?
Приклади
розв’язування типових задач
Електроліз
розплаву солей
Приклад 1. Які процеси окиснення-відновлення перебігають на катоді і на
аноді при електролізі розплаву NaCl з графітовими електродами?
Розв’язування: В
розплаві NаСІ дисоціює на йони:
NаСІ → 2Na+ +
2Cl- .
Катіони під дією електричного
струму будуть рухатись до катода і приймати від нього електрони
(відновлюватись). На аноді буде відбуватися процес окиснення хлорид-йонів:
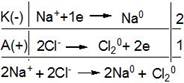
Таким чином, у результаті електролізу розплаву NaCl,
одержують Na і Сl2.
Приклад 2. Які окисно-відновні процеси перебігають на
інертних електродах при електролізі розплаву NaOH?
Розв’язування: У розплаві NaOH містяться Na+- і ОН--іони,
які рухаються відповідно до катоду і аноду. Процеси, які перебігають при цьому,
записують таким чином: NaОН → Na+ + ОН-.
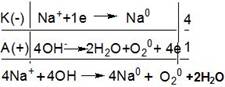
Таким чином, біля катоду
відновлюється натрій, а на аноді окиснюються ОН--іони (катодний і
анодний простір – відокремлені!).
Задача
№ 1.Визначте масу ртуті,
що виділилася під час пропускання постійного електричного струму силою 5 А
через розчин меркурій(ІІ) хлориду протягом однієї години.
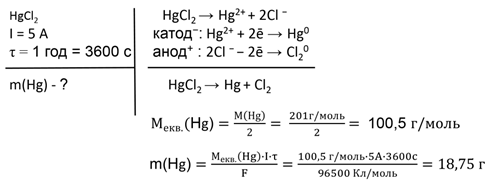
Відповідь: m(Hg) = 18,75 г.
Задача № 2.Визначте силу струму, при якій
з розчину аргентум нітрату можна отримати 27 г срібла за 10 хвилин.
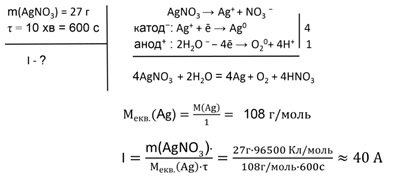
Відповідь.
I = 40 А.
Задача 3. Знайти електрорушійну силу (ЕРС)
элемента, утвореного цинковим електродом, опущеним в 0,1 М розчину нітрату
цинку і свинцевим електродом, опущенимм в 2 М розчин нітрату
свинцю.
Розв'язок.
ЕРС элемента дорівнює різниці
потенціалів електродів.
Розраховуємо потенціал цинкового електрода за
рівнянням Нернста:
EZn2+/Zn =
E0Zn2+/Zn + (0,059/n)*lg(CZn2+)
EZn2+/Zn =
-0,76 + (0,059/2)* (-1) = -0,79 В
Розраховуємо потенціал свинцевого електрода за
рівнянням Нернста:
EPb2+/Pb =
E0Pb2+/Pb + (0,059/n)*lg(CPb2+)
EPb2+/Pb =
-0,13 + (0,059/2)* 0.301 = -0,12 В
ЭЕРС = -0,12-(-0,79) = 0,67 В
Відповідь: 0,67
В.
Задача 4. Визначити, у якому напрямку можливе самодовільне
протікання реакції:
Cu +
ZnSO4 ![]() CnSO4 +
Zn
CnSO4 +
Zn
Розв’язування: Визначимо ступінь окислення
речовин, які беруть участь в окислювально-відновному процесі, окислювач і
відновник:
За таблицею стандартних
електродних потенціалів атомів у водних розчинах (див. додаток) знаходимо:
Е0 Cu0/Cu2+ =
+1,34 В,
Е0 Zn0/Zn2+ =
-0,76 В.
Для процесу, який протікає зліва
направо:
ΔЕ1° = Еок.°
– Евідн.° = -0,76-(0,34) = -1,1 В.
Для процесу, який протікає справа
наліво:
ΔЕ2° = Еок.°
– Евідн.° = 0,34 -(-0,76) = 1,1 В.
Позитивне значення ΔЕ2°
вказує на те, що дана реакція буде самодовільно протікати справа наліво (тобто
у даній системі Cu2+ — окислювач, Zn° — відновник).
Контрольні
завдання
1. Розв’язати задачі за
наведеною умовою
1. При електролізі розчину солі кадмію виділилося 2 г кадмію.
Яка кількість електричного струму затрачена при цьому, якщо me(Cd) =
= 56,25 г/моль.
2. Для виділення 1,75 г деякого металу з розчину його солі
потрібно пропустити струм силою 1,8 А протягом 1,5 год. Обчислити еквівалентну
масу металу.
3.За проходження через розчин солі двовалентного
металу електричного струму силою в
3 А протягом 2 годин на катоді виділилось 11,86 г металу.
Визначте цей метал.
4. Розрахуйте ЕРС гальванічного
елемента, який складається з залізного
електрода (Е0 Fe2+ /Fe=-0,44В) и срібного електрода (Е0Ag+/Ag=0,8В),
якщо концентрація (Fe2+)=0,01
моль/л, а концентрація (Ag+) = 0,01 моль/л. Наведіть схему
гальванічной пари.
5. Складіть схему
гальванічного елемента, який складається з
мідного і цинкового електродів, які поміщені в 0,01М
розчини солей цих металів. Розрахуйте ЕРС цього елемента. Напишіть рівняння
електродних процесів.

