Тема 2. Структура дорожньо-будівельних матеріалів.
1.
Атомно-молекулярна структура.
2.
Субмікроскопічна структура.
1.
Структура матеріалу – це будова його, визначена взаємним
розташуванням, формою, розмірами структурних елементів. Структурними елементами
можуть бути атоми, іони, молекули, тверді частинки різних розмірів
(дисперсності), агрегати частинок, пори (пустоти між частинками), заповнені
рідкою чи газоподібною фазою. Частинки – найдрібніші складові частини речовини,
які можна отримувати механічним шляхом (диспергуванням) або фізико-хімічними
засобами. Агрегати частинок утворюються внаслідок їх злипання, зокрема, зі
зростанням дисперсності та збільшенням поверхневої енергії, а також зрощення,
наприклад, у процесі кристалізації.
Структуру матеріалів, їх спільні
ознаки та особливості можна розглянути на різних рівнях залежно від розмірів
структурних елементів (l).
Виділяють чотири рівні структури будівельних матеріалів: атомно-молекулярний (l <
10-9м); субмікроскопічний (l =10-9...10-7м);
мікроскопічний (l
= 10-7...10-4м );
макроскопічний (l
>10-4м
).
Розглядаючи структуру матеріалу, на
атомно-молекулярному рівні вивчають: для кристалічних матеріалів –
особливості побудови елементарних комірок; для аморфних – особливості
агрегатів молекул, атомів або іонів, які не утворюють упорядковані ґратки. Ряд
матеріалів (цементи, полімери, шлаки) містять як кристалічні, так і аморфні
компоненти. Найстійкішим є кристалічний
стан тіла, оскільки енергія матеріалу при цьому мінімальна.
Структуру кристалів за
характеристиками міжатомних відстаней поділяють на 5 класів: координаційні
(відстані між структурними одиницями – атомами чи іонами – одного порядку), острівні
(містять групи відокремлених атомів, що утворюють “острови”), ланцюжкові
(містять відокремлені групи атомів, які утворюють суцільні ланцюги), шаруваті
(мають нескінченні у двох вимірах шари атомів), каркасні
(складаються з об’ємного тривимірного аніонового остова координаційного типу та
нейтралізуючої компоненти з аніонів чи атомних груп).
Через неоднакову щільність іонів або
атомів у різних площинах і напрямках властивості кристалів залежно від напрямку
неоднакові. Ця особливість кристалічних тіл називається анізотропією і
проявляється у ланцюжкових та шаруватих структурах.
Залежно від типу хімічного зв’язку між
структурними елементами розрізняють іонні, атомні (ковалентні), металеві,
молекулярні зв’язки і кристали з водневим зв’язком.
Іонний зв’язок
характерний для кристалів, які значно
відрізняються за електронегативністю їх структурних елементів. Більшість
катіонів має менший розмір, ніж аніони, і кристалічна ґратка іонних сполук
утворюється за рахунок розміщення катіонів у пустотах між аніонами.
Характерними властивостями іонних кристалів є низька електропровідність,
теплопровідність, крихкість та висока температура плавлення.
У вузлах атомних кристалічних ґраток
містяться нейтральні атоми, поєднані ковалентним зв’язком. Ці зв’язки
досить міцні. Речовини, які мають такі ґратки, тверді, тугоплавкі та практично
нерозчинні. Ковалентні кристали утворилися з атомів, які мають близькі значення
електронегативності. Якщо збільшується різниця в електронегативності елементів,
то зростає ступінь переходу ковалентного зв’язку в іонний. Кристали з
переважною кількістю ковалентних зв’язків мають вищу твердість порівняно з
кристалами з переважною кількістю іонних
зв’язків.
У металевих кристалах
визначальна роль належить електронам. Вони вільно переміщаються між атомами. У
вузлах таких кристалів коливаються позитивні іони металу, а валентні електрони
перебігають через ґратку в різних напрямках. Сукупність вільних електронів
іноді називається електронним газом. Така будова ґратки зумовлює високі тепло- і електропровідність і
пластичні властивості металів. Механічне деформування кристалічної ґратки в
певних межах не спричиняє руйнування кристалів, бо іони, що входять до їх
складу, ніби плавають у хмарі електронного газу.
У вузлах молекулярних кристалічних
ґраток розміщені групи атомів чи
молекули, пов’язані між собою Ван-дер-Ваальсівськими силами та дипольними
взаємодіями. Сили Ван-дер-Ваальса зростають у разі, коли збільшується кількість
атомів у молекулі та їх полярність. Молекулярні сили порівняно слабкі, тому
молекулярні кристали, що характерні для ряду органічних речовин, легкоплавкі,
леткі і мають низьку твердість.
Поширений тип зв’язку у кристалах
неорганічних речовин – зв’язок через іон водню, що є між двома аніонами і міцно
пов’язує їх. Утворення водневого зв’язку має велике значення у
структурах води і багатьох інших сполук, до складу яких входять водень і
кисень. Водневим зв’язком значною мірою пояснюються аномальні властивості води:
висока діелектрична стала, поверхневий натяг, здатність до змочування і
розчинення багатьох речовин. Виникнення водневого зв’язку пояснюється тим, що
атом водню, віддаючи свій єдиний електрон на утворення ковалентного зв’язку з
киснем і залишаючись ядром відносно малих розмірів з досить сильним електричним
полем, активно взаємодіє з електронними оболонками атомів кисню в молекулах
інших речовин. Водневі зв’язки
зумовлюють полімеризацію деяких органічних кислот і сприяють утворенню
багатьох неорганічних полімерів. Виникнення водневого зв’язку частково зумовлює
гідратацію полярних груп. А також гідрофільність відповідних поверхонь
матеріалів.
У більшості кристалів водночас діє
кілька типів зв’язків, з урахуванням
характеру яких оцінюють їх теоретичну міцність і інші властивості.
Здатність атомів, іонів або молекул
заміщати один одного в кристалічних структурах і утворювати при цьому гомогенні
фази змінного складу називають ізоморфізмом. Ізоморфізм може
відбуватися, якщо атоми мають однакові координаційні числа, а також за умови
близьких розмірів іонів, що взаємо заміщуються, однакової будови їх електронних
оболонок.
Тверді розчини проникнення належать до
твердих розчинів, що характеризуються змінним складом. Як правило, через
міжвузловини здатні проникати атоми та іони невеликих розмірів або сумірні з
пустотами кристалічної ґратки. Найчастіше розчини проникнення трапляються у
металевих матеріалах. Поряд з твердими розчинами заміщення та проникнення
існують тверді розчини вилучення, які характеризуються незаповненими
структурними позиціями.
Основними видами лінійних дефектів
кристалів є дислокації, уздовж і поблизу яких порушується порядок у
розташуванні атомних площин. Розрізняють крайові та гвинтові дислокації.
Крайова дислокація є локалізованим спотворенням кристалічної ґратки,
спричиненим наявністю в ній “зайвої” атомної напівплощини. Гвинтова дислокація
– лінія, утворена атомними площинами у вигляді гвинтової поверхні. Дислокація
утворюється внаслідок зсуву частин кристала вздовж площини ковзання,
паралельної одній з площин кристалічної ґратки.
Під дією дотичних напружень дислокації
можуть рухатися, за рахунок чого в кристалах виникають пластичні деформації.
Дислокації є джерелами внутрішніх напружень, ділянки кристала поблизу них
перебувають у пружно-напруженому стані. Навіть незначна кількість дислокацій
може знизити міцність матеріалів на декілька порядків.
Дуже високу міцність, що наближається
до теоретичної, мають ниткоподібні кристали, які завдяки такій структурі мають
невелику кількість дислокацій. Ці кристали можуть бути ефективними
мікроармуючими матеріалами. В деяких випадках зміцнення матеріалів досягають
введенням легуючих добавок, які запобігають руху дислокацій.
Структура аморфних матеріалів,
як і структура рідин, характеризується
так званим близьким порядком, коли упорядкований стан спостерігається
тільки між сусідніми частинками матеріалу. До головних відмінних особливостей
аморфних, у тому числі склоподібних, структур, належить ізотропність властивостей та відсутність сталої
температури плавлення. Відсутність кристалічної ґратки веде до плавної зміни
властивостей аморфних матеріалів при переході їх, наприклад, з твердого стану в
рідкий. Аморфні тіла можна розглядати як переохолоджену рідину, проте, на
відміну від рідин, у них не відбувається швидкого обміну місцями між сусідніми
частинками, що зумовлює їх високу в’язкість.
До найважливіших методів дослідження
структур матеріалів належать рентгенівські методи. Рентгенівські промені
проходять через кристалічні ґратки і зазнають дифракції, оскільки міжатомні
відстані в них сумірні з довжиною хвиль рентгенівського випромінювання. Кожен
кристал на рентгенограмах дає характерні лінії, які відрізняються розташуванням
та інтенсивністю. Розшифрування рентгенограм дає змогу визначити характер
дефектів, тип елементарної комірки, положення атомів або іонів та інші
особливості структури атомно-молекулярного рівня структури матеріалів.
Електронно-графічний
аналіз ґрунтується на використанні електронних хвиль, які мають довжину на
один-два порядки меншу за рентгенівські хвилі і тому здатні проникати у ґратку
на глибину до 10 атомних шарів. Електронні хвилі отримують у закритій скляній
трубці з вакуумом за рахунок пучка електронів від розжареної струмом високої
напруги нитки вольфрамового сплаву.
Спектроскопічні методи дослідження
структури матеріалів засновані на квантових уявленнях. Рентгенівську
спектроскопію застосовують, вивчаючи енергетичні особливості
атомно-молекулярної структури і проводячи хімічний експрес-аналіз.
2. На
субмікроскопічному рівні розглядають структури матеріалів, утворені частинками
колоїдних розмірів (10-9...10-7м) і які можна розрізняти
у звичайному світловому мікроскопі. У дисперсних системах одна чи кілька
речовин є дрібними частинками або порами, розподіленими у навколишньому
дисперсійному середовищі.
Дисперсність
системи характеризує площа питомої поверхні S, під якою розуміють
відношення загальної площі F
дисперсної фази до її загального об’єму V: S = F/V.
Дисперсні системи належать до трьох
основних груп, які відрізняються фазовим складом дисперсійного середовища – твердим,
рідким, газоподібним. Дисперсні фази в системах кожної групи також можуть
перебувати в трьох агрегатних станах.
У будівельних матеріалах, які належать
до дисперсних систем, дисперсну фазу найчастіше складають тверді частинки. Це
різноманітні порошки, суспензії, пасти, пластично-в’язкі рідиноподібні суміші,
в’яжучі речовини, пластмаси, лакофарбові суміші, керамічні маси, розчини та
бетонні суміші, розплави склоподібних речовин тощо. У деяких матеріалах
дисперсна фаза може бути рідкою (полімерні емульсії) або газоподібною (пористі
гірські породи, ніздрюваті бетони, піноскло, пінопласти тощо).
До поверхнево-активних речовин
належать речовини здебільшого органічного походження, до молекул яких входять
полярні і неполярні групи. У технології
будівельних матеріалів широко використовується явище адсорбції ПАР на твердих
поверхнях, у результаті чого змінюється їх змочуваність відносно рідин,
зменшується твердість, поліпшується пластичність.
Внаслідок зчеплення невпорядковано
розподілених твердих частинок дисперсної фази в суспензіях та колоїдних
розчинах утворюється просторова сітка – коагуляційна структура.
Утворення таких структур характерне для
багатьох матеріалів, наприклад, на основі в’яжучих речовин у перший період їх
твердіння. Характерною ознакою їх твердіння й утворення коагуляційної структури
є наявність обернених контактів, тобто довільно відновлюваних після руйнування
коагуляційних контактів. Міцність цих контактів зумовлена слабкими
Ван-дер-Ваальсівськими молекулярними силами зчеплення крізь найтонші прошарки
дисперсійного середовища, товщина якого відповідає мінімальному значенню
поверхневої енергії.
Сила зв’язку коагуляційних контактів
різко зменшується, якщо поверхні частинок вкриті шаром ПАР. Адсорбуючись, ПАР
розсувають частинки щонайменше на відстань двох молекулярних шарів, екрануючи
енергетично найактивніші ділянки
частинок. Коагуляційні структури називають гелями. Під гелеутворенням
розуміють перехід колоїдного розчину з вільнодисперсного стану у
зв’язнодисперсний (гель).
На гелеутворення (процес коагуляції)
впливають різні фактори, зокрема, форма частинок, концентрація дисперсної фази,
температура суміші, види механічних дій
(змішування, вібрування). Коагуляцію спричиняють електроліти, які містять іони протилежного
знака відносно колоїдної частини.
Розрізняють дві форми коагуляції –
явну і приховану. У разі явної коагуляції система поділяється на дві
макроскопічні фази – осад і рідке середовище. У прихованій коагуляції
агрегатування частинок можна виявити тільки спеціальними методами, наприклад,
за зміною електрокінетичного потенціалу.
Процес, зворотний до колоїдації, тобто
перехід агрегатованих частинок у вихідний колоїдний стан, називається пептизацією.
Механізм пептизації полягає у вилученні з осадів коагулюючих іонів або
утворенні у колоїдних частинок подвійних електричних шарів внаслідок адсорбції
ними пептизатора.
Коагуляційні структури розріджуються
також під впливом механічних дій при
змішуванні, струшуванні чи вібруванні.
Цей ізотермічний процес називають тиксотропією. Після припинення
механічних дій зв’язки, порушені в коагуляційній структурі, відновлюються.
Тиксотропію використовують для вібраційного ущільнення бетонних сумішей.
Властивості колоїдних розчинів можна
пов’язати з їх міцелярною будовою. Міцела – найменша кількість колоїдної
речовини, що є складним утворенням, у якому частинки дисперсної фази (ядро)
перебувають у певному фізико-хімічному зв’язку з розчином через подвійний
електричний шар іонів (рис. 1.1).
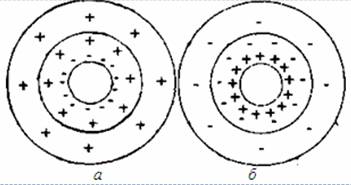
Рис. 1.1. Будова
міцели:
а – з від’ємно зарядженою частинкою;б – з позитивно
зарядженою частинкою
Вплив міцелярної будови відчутно позначається на
властивостях будівельних матеріалів. Наприклад, тверда дисперсна фаза бітуму –
асфальтени – утворює ядра, оточені оболонкою рідкого середовища – від важких
смол до порівняно легких масел. У разі надлишку рідкого середовища міцели не
контактують між собою і вільно пересуваються під впливом броунівського руху.
3. На мікроскопічному
рівні вивчають елементи структури матеріалів, які можна виявити за допомогою
оптичного чи електронного мікроскопа. Їх розміри становлять 10-4...10-7м,
вони характерні для мікрогетерогенних систем.
Типові мікрогетерогенні системи
– це порошки, суспензії, емульсії і піни. Для цих систем, на відміну від
колоїдних, броунівський рух не характерний. Частинки в них переміщуються під
впливом ваги, тому вони седиментаційно нестійкі.
Порошки,
які широко використовуються у будівельних матеріалах, можна розглядати як
дисперсні системи, дисперсійним середовищем де є повітря. Порошки отримують методом
подрібнення. Дисперсність порошків контролюють за площею питомої
поверхні і зерновим складом.
Для визначення зернового складу
порошків використовують ситовий та седиментаційний аналізи. Седиментаційний
аналіз пов’язаний з тим, що швидкість осідання частинок у рідкому середовищі
змінюється залежно від їх розмірів.
Зменшення розмірів зерен у порошках
нижче критичного рівня спричинює їх
злипання та гранулювання. Гранулювання порошків відбувається
завдяки зменшенню поверхневої енергії системи при злипанні частинок.
Активізації цього процесу сприяє змочуваність поверхні твердої фази рідиною. Це
забезпечує утворення на межі поділу прошарку з підвищеною в’язкістю, що
збільшує адгезійну взаємодію.
Суспензії та
емульсії – це мікрогетерогенні системи, в яких тверда або рідка дисперсні
фази розподілені у рідкому дисперсному середовищі. У виробництві будівельних
матеріалів суспензії широко використовують при отриманні сировинних шламів,
шлікерів, розчинів. Емульсії
застосовують зокрема як лакофарбові матеріали. Концентровані суспензії
називають пастами.
Як будівельні матеріали широко
застосовують емульсії на основі органічних в’яжучих речовин – бітуму, дьогтю,
полімерів тощо.
Бітумні емульсії бувають аніонними
(виготовляють на аніонних ПАР – вищих органічних кислотах, їх лужних милах) та катіонними
(на емульгаторах катіонного типу – солях амінів, амідно-амінних милах). Частіше
і простіше готувати бітумні пасти, що є концентрованими дисперсними системами з
бітуму, води й твердого емульгатора (вапно, цемент, пластична глина).
Піни
– висококонцентровані системи, в яких дисперсна фаза – газ, дисперсне
середовище – рідина, розтягнута у тонкі плівки. Як теплоізоляційні матеріали
застосовують тверді піни, в яких перетинки між газовими бульбашками подані
твердою фазою (пінопласти, піноскло, пінобетон, газобетон). Для отримання
стійких пін використовують піноутворювачі – високомолекулярні речовини, мила
тощо.
Найважливішими елементами
мікроструктури матеріалів, що визначають їх властивості є пори.
Найдрібніші пори (ультрамікропори) виникають внаслідок анізотропії властивостей
кристалів і частинок конденсаційних структур, а також їх випадкової орієнтації
у просторі у процесі росту. Крупніші пори штучних матеріалів здебільшого
технологічного походження. Вони виникають внаслідок нещільного укладання
суміші, защемлення повітря, випаровування надлишкової води, деструктивних
процесів вилужування, дегідратації, вивітрювання тощо.
4.
На макроскопічному рівні структуру матеріалів розглядають, якщо розміри
частинок становлять понад 10-4 м. Макроструктуру вивчають
неозброєним оком чи у разі незначного збільшення. При цьому можна визначити особливості
будови та дефектів матеріалів, зумовлених процесами їх формування, виробництва
та експлуатації (наприклад, дефекти ливарного походження у металів, вади
деревини, бульбашки повітря та сторонні включення у склі, тріщини та раковини у
бетоні тощо).
Вивчення макроструктури матеріалів
конгломератного типу дає змогу визначити відносну кількість в’яжучого матеріалу
та заповнювачів, їх розподіл, мінералогічних склад, розмір і форму зерен,
характер поверхні, форму і кількість макропор.
Структура будівельних матеріалів з
часом змінюється під впливом процесів, зумовлених як внутрішньою їх природою,
так і навколишнім середовищем. Ці процеси можуть бути як конструктивними,
що поліпшують структуру і властивості матеріалу, так і деструктивними,
які спричиняють зворотну дію. На розвиток деструктивних процесів впливають
дефекти структури матеріалів – пори, тріщини тощо. Найнебезпечнішими порами є
капіляри, заповнені водою.
Тріщини
– невід’ємні елементи структури будівельних матеріалів, які можна розглядати як
порушення їх суцільності. Вони мають дві вільні поверхні, що, змикаючись,
утворюють гостру вершину. Тріщини виникають внаслідок механічної,
електрохімічної, термічної чи іншої обробки матеріалу. За походженням тріщини
поділяють на силові, усадкові, температурні, корозійні. Загальною
характеристикою тріщин є їх довжина, глибина, ширина розкриття, форма
поперечного та поздовжнього перерізів.
Тріщини суттєво знижують міцність
матеріалів. Вони є “воротами агресії”. Особливо небезпечні тріщини у крихких
матеріалах та у конструкціях, які піддаються циклічному навантаженню. Тріщини
виявляють за допомогою візуального огляду, ультразвуковою та магнітною
дефектоскопією, люмінесцентними рідинами, просвічуванням тощо.

